Índice
Hum Genet. 2012 Oct; 131(10): 1565–1589.
Published online 2012 Jun 28. doi: 10.1007/s00439-012-1189-8
PMCID: PMC3432200
PMID: 22740325
Epigenética ambiental: perspectivas para estudiar la mediación epigenética de las relaciones de exposición-respuesta
Victoria K. Cortessis,1 Duncan C. Thomas,2 A. Joan Levine,1 Carrie V. Breton,3 Thomas M. Mack,1 Kimberly D. Siegmund,3 Robert W. Haile,1 and Peter W. Laird4
Author information Article notes Copyright and License information Disclaimer
This article has been cited by other articles in PMC.
https://link.springer.com/article/10.1007/s00439-012-1189-8
https://link.springer.com/content/pdf/10.1007%2Fs00439-012-1189-8.pdf
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3432200/
Resumen
Los cambios en las marcas epigenéticas, como la metilación del ADN y la acetilación de histonas, están asociados con una amplia gama de características de la enfermedad, que incluyen cáncer, asma, trastornos metabólicos y diversas afecciones reproductivas. Parece plausible que los cambios en el estado epigenético puedan ser inducidos por exposiciones ambientales como la desnutrición, el humo del tabaco, los contaminantes del aire, metales, sustancias químicas orgánicas, otras fuentes de estrés oxidativo y el microbioma, especialmente si la exposición ocurre durante los períodos clave de desarrollo. Por lo tanto, los cambios epigenéticos podrían representar una vía importante por la cual los factores ambientales influyen en los riesgos de la enfermedad, tanto dentro de los individuos como a través de las generaciones. Discutimos algunos de los desafíos en el estudio de la mediación epigenética de la patogénesis y describimos algunas oportunidades únicas para explorar estos fenómenos.
Antecedentes
El campo de la epigenética creció a partir de los intentos, que comenzaron hace más de 70 años, para comprender los mecanismos por los cuales múltiples fenotipos celulares surgen de un solo genotipo durante el complejo proceso de morfogénesis del desarrollo denominado epigénesis. El término “epigenética” se reservó inicialmente para los mecanismos por los cuales el estado fenotípico, según lo determinado por la expresión génica diferencial, podría retenerse de manera estable a través de la división celular por factores no genéticos. Se han propuesto varios mecanismos para tener el potencial de codificar esta información fenotípica; estos incluyen la metilación enzimática de las bases de citosina (metilación del ADN), la modificación postraduccional de los dominios de la cola de las proteínas histonas (modificaciones de las histonas) y el posicionamiento del nucleosoma asociado o la remodelación de la cromatina, los ARN no codificantes y las redes reguladoras del factor de transcripción (Ptashne 2007). Las marcas epigenéticas establecidas por cada uno de estos procesos a menudo se comparten dentro de un linaje celular; sin embargo, si todas las marcas epigenéticas persistentes satisfacen los requisitos para una transmisión estable a través de la división celular o algunas simplemente se restablecen a partir de otra información después de la mitosis, sigue siendo una cuestión que se debate con fuerza.
El término epigenética se ha utilizado más recientemente en la literatura científica para describir diversos mecanismos no genéticos no especificados que influyen en el fenotipo. Este uso más amplio surgió de estudios con ratones que abordaban los efectos nutricionales transgeneracionales sobre el fenotipo, así como estudios en humanos sobre las diferencias fenotípicas entre gemelos monocigóticos. En la prensa popular, “epigenética” se ha convertido casi en sinónimo de influencias nutricionales y ambientales en la expresión génica. Así, mientras que la “epigenética” se refería inicialmente a procesos de desarrollo en gran parte autocontenidos, ha llegado a describir influencias ambientales en la lectura fenotípica de genotipos. Esta evolución semántica ha causado confusión y controversia sobre el significado de “epigenética” en un momento de mayor interés en el posible papel de los mecanismos epigenéticos en la enfermedad. En esta revisión, definimos como procesos epigenéticos aquellos que afectan de manera estable la expresión génica a través de mecanismos que no involucran la secuencia de nucleótidos primaria, y el estado epigenético como la configuración de cromatina y marcas de ADN utilizadas por estos procesos. Por el contrario, se entiende ampliamente que el estado genético se refiere a la secuencia de nucleótidos primaria, mientras que los procesos genéticos mantienen o cambian la secuencia de nucleótidos.
La investigación epidemiológica que aborda los mecanismos epigenéticos como mediadores de las exposiciones ambientales al riesgo de enfermedad se ve limitada por importantes consideraciones éticas. Estos a menudo excluyen tanto la exposición experimental a causas ambientales candidatas como la recolección invasiva de tipos de células de mayor relevancia funcional y de desarrollo para los procesos de enfermedades. Por lo tanto, la investigación ha progresado en gran medida al integrar información sobre los mecanismos biológicos obtenidos en sistemas modelo con datos de observación proporcionados por humanos. Para abordar el estado actual y la promesa futura de esta investigación, emprendimos esta revisión con dos objetivos: ilustrar el potencial de los procesos epigenéticos para mediar las relaciones de exposición-fenotipo y discutir el diseño del estudio y los métodos de análisis estadístico necesarios para investigar dichos mecanismos en relación con Orígenes de la enfermedad humana. Comenzamos discutiendo los determinantes genéticos, de desarrollo y ambientales del estado epigenético en los sistemas humanos y modelos, luego describimos algunos de los diversos datos que implican mecanismos epigenéticos en diversas enfermedades humanas, tanto dentro de individuos como a través de generaciones. Concluimos discutiendo los desafíos técnicos, sugiriendo oportunidades prometedoras para la investigación epidemiológica en epigenética ambiental y ofreciendo algunas reflexiones sobre la importancia de la traducción y las direcciones futuras de este campo.
Determinantes del estado epigenético.
Los mecanismos epigenéticos funcionan en conjunto para influir en el potencial de la expresión génica en innumerables ubicaciones en todo el genoma. El estado epigenético resultante del genoma, denominado epigenoma, varía según el tipo de célula. Teniendo en cuenta la tremenda diversidad de marcas epigenéticas, que incluyen docenas de diferentes modificaciones de histonas postraduccionales y más de 50 millones de sitios de potencial metilación de ADN en un genoma humano diploide (¡y por lo tanto> 250M posibles epigenotipos!), Parece que no hay dos células humanas que tendrían epigenomas idénticos. De hecho, dentro de cada individuo hay muchos epigenomas, y estos cambian con el tiempo como consecuencia de los procesos patológicos y de desarrollo normales, así como de las exposiciones ambientales y la deriva aleatoria. A pesar de este potencial para una considerable variabilidad de los patrones epigenéticos dentro y entre individuos, también puede haber una consistencia notable. En un estudio de 11 tejidos en 6 autopsias, se encontró que los patrones de metilación del ADN en un conjunto altamente seleccionado de loci estaban altamente conservados, con correlaciones intraclase de 0,85 entre los tejidos dentro de los individuos y 0,83 entre los individuos dentro de los tejidos (Byun et al. 2009). Los autores interpretaron estos patrones como reveladores de diferentes conjuntos de genes metilados diferencialmente específicos de la persona y del tejido, anticipando la determinación genética y adquirida diferencial observada posteriormente (Waterland et al. 2010).
La metilación del ADN ha sido la marca epigenética más ampliamente medida en la investigación epidemiológica por numerosas razones. Es de interés biológico fundamental debido a su transmisión inequívocamente estable durante la división celular. También tiene ventajas prácticas: como un cambio covalente químicamente estable al ADN mismo, la metilación del ADN es la única marca epigenética que sobrevive a la extracción y purificación de ADN que es de rutina en el procesamiento de muestras moleculares, y puede soportar décadas de almacenamiento de muestras en archivos (Kristensen et al. 2009).
Influencias genéticas
Programación evolutiva del epigenoma.
En la reproducción exitosa de los mamíferos, el cigoto unicelular da lugar a un organismo con cientos de tipos de células. Estos diversos fenotipos celulares surgen de la misma secuencia genómica compartida por el control del subconjunto de genes expresados en cada tipo de célula. La diferenciación celular está estrechamente vinculada al extenso borrado y al establecimiento de marcas epigenéticas específicas del linaje, un proceso denominado reprogramación epigenética. Se han llevado a cabo descripciones relativamente detalladas de la metilación del ADN en tejidos en desarrollo en el ratón, que sirve como modelo de reprogramación epigenética en el desarrollo de los mamíferos (Trasler 2009).
En la fertilización, la reprogramación comienza con un extenso borrado de las marcas de metilo en el ADN del ADN paterno (derivado de esperma), seguido de una pérdida más general de las marcas de metilo en el cigoto y el embrión durante las divisiones de escisión, a la vez que se evitan las huellas específicas del padre de origen. Por la etapa del blastocisto, la metilación del ADN de novo distingue a las células de la masa celular interna (de las cuales surgen linajes embrionarios para crear estructuras fetales) de las células del trofectodermo relativamente hipometiladas (de las cuales surgen linajes extraembrionarios para crear estructuras transitorias, incluida la placenta) (Fig. 1 ).
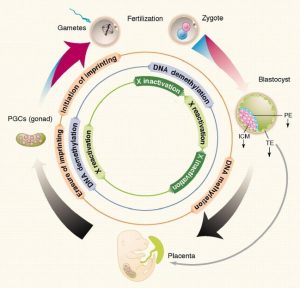
Reprogramación de la metilación del ADN en el cigoto, embrión temprano y células germinales primordiales. El grosor de las flechas externas indica los niveles de metilación del ADN. Genoma materno rojo, genoma paterno azul, genoma diploide negro. Los linajes embrionarios surgen de las células de la masa celular interna (ICM), la placenta y las membranas extraembrionarias de las células del trofectodermo, y el linaje de las células germinales de las células germinales primordiales después de su determinación a partir del epiblasto proximal. Los círculos internos indican etapas de desarrollo cuando se cree que ocurren elementos clave de la programación epigenética (Adaptado de Feng et al. 2010)
La especificación del linaje de las células germinales comienza en las células del epiblasto proximal, e implica un segundo borrado extenso de la metilación del ADN que elimina las marcas de impresión de los padres (Fig. 1). A partir de entonces, la línea germinal se desarrolla de forma dimórfica sexual. Se establecen nuevas marcas de metilo en el ADN en muchas etapas, que se extienden a través de la madurez sexual de acuerdo con el sexo del individuo en desarrollo. En este momento, se establecen las marcas de impresión específicas del sexo que rigen la expresión específica del origen de los genes impresos en la generación posterior (Faulk y Dolinoy 2011).
La reprogramación del desarrollo puede dar lugar a diferencias epigenéticas dramáticas entre los dos alelos. La asociación entre la expresión de genes mono-alélicos y la metilación del ADN ha sido reconocida durante mucho tiempo, tanto en el contexto de la inactivación de X en hembras (Boggs et al. 2002; Sharp et al. 2011) como en la impronta genómica determinada por el padre de origen ( Ferguson-Smith 2011), pero ahora también en la expresión mono-alélica de loci autosómicos no impresos (Harris et al. 2010; Tarutani y Takayama 2011).
El restablecimiento adicional de las marcas epigenéticas acompaña a la diferenciación de muchos tipos de células especializadas del cuerpo, así como a la placenta y otras estructuras transitorias durante el embarazo, y el desarrollo posterior de las estructuras corporales durante varias etapas postnatales del desarrollo. Los estados de cromatina que surgen durante el desarrollo pueden afectar la propensión al cambio epigenético posterior. Un ejemplo de esto es la predisposición de los genes ocupados por el complejo poliquor-represivo en las células madre a la adquisición de anomalías de metilación del ADN en el envejecimiento y el cáncer (Ohm et al. 2007; Schlesinger et al. 2007; Teschendorff et al. 2010; Widschwendter et al . 2007).
Influencias ambientales
Estudios experimentales
Estudios humanos
Christensen y Marsit (2011) y Terry et al. (2011) han proporcionado revisiones exhaustivas de las influencias ambientales en el estado epigenético en los seres humanos. Aquí observamos periodos de exposición de particular interés y varios ejemplos de exposiciones ambientales que según se informa están asociadas con el estado epigenético de tipos de células humanas específicas.
El epigenoma puede ser más vulnerable a las agresiones ambientales durante los períodos de reprogramación epigenética extensa, que en teoría puede verse interrumpida por exposiciones que interfieran con cualquier proceso que gobierne la reprogramación. Por lo tanto, los períodos de vulnerabilidad particular pueden incluir las etapas iniciales del desarrollo embrionario mencionadas anteriormente. La infancia también se propone como un período de vulnerabilidad, especialmente en la línea germinal de las hembras, ya que los ovocitos permanecen en estado haploide desmetilado hasta la pubertad, por lo que los insultos ambientales pueden perturbar potencialmente el estado epigenético del ovocito durante muchos años (Faulk y Dolinoy 2011 ), con implicaciones potenciales tanto para la fertilidad como para el estado epigenético inicial de la descendencia de una hembra expuesta. Los cambios somáticos en la metilación del ADN también pueden deberse a exposiciones ambientales en adultos, como se ha observado en procesos de envejecimiento y enfermedades como el cáncer que se describen en la siguiente sección.
Ingesta energética y de nutrientes.
Se han documentado cambios epigenéticos significativos en el gen IGF2 en aquellos expuestos prenatalmente a una restricción calórica severa durante el invierno del hambre holandés de la Segunda Guerra Mundial (Heijmans et al. 2008). Hughes et al. (2009), además, encontraron que las personas con mayor probabilidad de estar expuestas a esta hambruna durante la adolescencia o la adultez joven tenían un riesgo significativamente menor de desarrollar cánceres colorrectales (CCR) caracterizados por el fenotipo metilante de la isla CpG (CIMP), lo que sugiere un papel para las exposiciones tempranas en la vida en la patogénesis de CRC específica de CIMP.
Los folatos son la fuente principal de los grupos metilo utilizados para la metilación del ADN y las histonas. Un estudio de folatos y otros nutrientes de un solo carbono informó un efecto diferencial del folato sobre el riesgo del subconjunto de CRC de CIMP en comparación con el subconjunto no de CIMP (Van Guelpen et al. 2010), mientras que otros dos estudios no (Slattery et al. . 2006; van den Donk et al. 2007). La mayoría de los estudios del subconjunto de inestabilidad de microsatélites, caracterizado por hipermetilación de la región promotora del gen MLH1 y CIMP (Weisenberger et al. 2006), arrojaron resultados igualmente negativos (Eaton et al. 2005; Schernhammer et al. 2008; Slattery et al. 2001; Wark et al. 2005). Por otro lado, en algunos estudios, se ha informado que la asociación entre la ingesta de alcohol (que degrada los folatos) y el riesgo de CCR es mayor en los tumores MSI-H y CIMP (Diergaarde et al. 2003; Eaton et al. 2005; Slattery et al. al. 2001).
Los micro-ARN (miARN) son moléculas de ARN no codificantes muy cortas que pueden regular a la baja los genes codificantes de proteínas desestabilizando los ARNm o bloqueando la traducción. La posibilidad de que el microARN exógeno consumido en los alimentos pueda regular de manera epigenética la expresión génica ha surgido de estudios recientes que demuestran la presencia de miARNs derivados de plantas en sueros de humanos y otros mamíferos (Zhang et al. 2012). Uno de estos microRNAs de plantas, MIR168a, que se demostró que solo es de origen vegetal en ratones de control, se une a la secuencia codificante del gen LDLRAP1 de mamíferos in vitro. Las consecuencias funcionales en sistemas de mamíferos se demostraron experimentalmente, ya que MIR168a administrado in vitro y durante los estudios de alimentación in vivo disminuyó la expresión del producto proteico de LDLRAP1. Esta línea de investigación sugiere nuevos mecanismos epigenéticos mediante los cuales la dieta puede modificar el riesgo de enfermedad humana.
La contaminación del aire
La evidencia emergente sugiere que los contaminantes del aire pueden influir en los cambios epigenéticos, incluida la metilación del ADN, así como la regulación hacia arriba o hacia abajo de los miRNA (Jardim, 2011). En estudios epidemiológicos en humanos, las exposiciones a PM2.5 y PM10 se asocian con la hipometilación de elementos Alu y / o LINE1 en leucocitos y células bucales (Baccarelli et al. 2009; Bollati y Baccarelli 2010; Madrigano et al. 2011; Salam et al. 2012 ; Tarantini et al. 2009), así como alteración de la metilación del ADN en NOS2A, un gen involucrado en la producción de óxido nítrico (Salam et al. 2012; Tarantini et al. 2009). Vivir en ciudades altamente contaminadas (alto PM y ozono) también se asocia con hipermetilación de FOXP3 en células T reguladoras (Nadeau et al. 2010), mientras que los neonatos que fueron expuestos prenatalmente a hidrocarburo poliaromático (HAP) tenían ACSL3 hipermetilado en el ADN del cordón umbilical glóbulos blancos (Perera et al. 2009); En particular, ambos genes están involucrados en la patogénesis del asma. Los HAP también están asociados con la hipermetilación de LINE1 y Alu (Pavanello et al. 2009; Perera et al. 2009). Aparecen evidencias más limitadas que sugieren que la contaminación del aire está asociada con cambios en la expresión de miRNA (Bollati et al. 2010; Jardim 2011), y los efectos adversos de los componentes de la contaminación del aire pueden modificarse por alelos variantes de genes involucrados en el procesamiento de miRNA (Wilker et al. al. 2010).
Humo de tabaco
La exposición fetal al tabaquismo materno durante el embarazo (PTS) se asocia con una reducción de la metilación de varias secuencias repetidas, incluidas Sat2 (Flom et al. 2011), Alu y LINE1 entre niños con el genotipo nulo GSTM1 (Breton et al. 2009). La exposición a PTS también se asocia con un aumento de la metilación del ADN en genes específicos, como AXL y PTPRO (Breton et al. 2009, 2011b) e IGF2 (Murphy et al. 2011). En pacientes adultos con cáncer de pulmón, la cantidad y la duración del tabaquismo activo, así como el humo de segunda mano, se asocian con un aumento de la metilación del ADN de p16 (Kim et al. 2001; Scesnaite et al. 2012), MGMT y DAPK (Russo et al. 2005). El humo del tabaco también se asocia con cambios en la metilación del ADN de las células tumorales en el carcinoma de células escamosas esofágicas (Huang et al. 2011), frecuencias significativamente más altas de hipermetilación anormal del ADN en la próstata (Enokida et al. 2006) y células tumorales de cáncer gástrico (Nan et al. 2005) y con un mayor riesgo de tumores colorrectales CIMP + (Limsui et al. 2010; Samowitz et al. 2006). Por último, el gen F2RL3 está hipometilado en los fumadores y puede mediar el impacto perjudicial del hábito de fumar en la mortalidad cardiovascular, ya que se encontró que el F2RL3 hipometilado estaba fuertemente asociado con la mortalidad cardiovascular entre los pacientes con enfermedad coronaria estable (Breitling et al. 2012).
Estrés oxidativo
Las especies reactivas de oxígeno (ROS) están involucradas en numerosos procesos celulares que incluyen alteraciones redox celulares, respuesta inmune, vías de señalización, remodelación de cromatina y expresión génica (Sundar et al. 2010). Las ROS tienen el potencial de influir en los mecanismos epigenéticos (Baccarelli y Bollati 2009), y se ha demostrado que inhiben la unión de la proteína 2 de unión a la metil-CpG, un regulador epigenético crítico que recluta a la citosina metil transferasas y las histonas desacetilasas al ADN (Valinluck et al. 2004). ). Numerosas exposiciones ambientales, incluidos los constituyentes de la contaminación del aire y el humo del tabaco, pueden generar ROS y, por lo tanto, pueden alterar los procesos epigenéticos a través de mecanismos de estrés oxidativo.
Metales
La exposición prenatal al plomo se asocia con una disminución de la metilación de LINE1 y Alu en la sangre del cordón umbilical (Pilsner et al. 2009), y se informó un patrón similar de metilación de LINE1 en una cohorte de ancianos (Wright et al. 2010). Los estudios en humanos han demostrado que la exposición al arsénico está asociada con la hipermetilación global o la hipometilación en células mononucleares de sangre periférica (PBMC) según la dosis (Majumdar et al. 2010), así como la hipermetilación del ADN de varios genes, incluido el CDKN2A (Chanda et al. . 2006), RASSF1A y PRSS3 (Marsit et al. 2006).
Interacciones genéticas × epigenéticas × ambientales
La mayoría del trabajo que investiga los efectos de los factores ambientales en el estado epigenético no ha considerado el potencial de susceptibilidad genética para modificar estas asociaciones. Sin embargo, Salam et al. (2012) investigaron recientemente las contribuciones de la variación tanto genética como epigenética en los niveles mediados por la contaminación del aire de óxido nítrico exhalado fraccional (feNO). La medición de feNO proporciona una evaluación resumida in vivo de la actividad de la sintetasa de óxido nítrico inducible (iNOS), así como la inflamación de las vías respiratorias. Estos investigadores encontraron efectos interrelacionados de la exposición a los componentes de la contaminación del aire PM2.5, los haplotipos promotores NOS2A y la metilación del gen que codifica iNOS NOS2A y los haplotipos promotores NOS2 a nivel de feNO. Estas observaciones ilustran no solo la viabilidad de evaluar las interacciones entre factores epigenéticos, genéticos y ambientales, sino también la importancia de hacerlo para delinear relaciones biológicas complejas e identificar subpoblaciones susceptibles.
Efectos epigenéticos en la enfermedad humana.
Las condiciones asociadas con la contribución parental inadecuada de los genes impresos son actualmente los ejemplos más claros de enfermedades humanas relacionadas con el estado epigenético.
El papel de la epigenética en la mayoría de las otras condiciones sigue siendo mucho menos claro. Sin embargo, dado que Barker propuso que a veces existe una base fetal para la enfermedad en adultos (Barker et al. 1993), la investigación epidemiológica ha implicado que numerosas exposiciones ambientales durante el desarrollo prenatal y postnatal temprano influyen en el riesgo de enfermedad cardiovascular en adultos, obesidad, diabetes tipo 2, y otras afecciones crónicas (Taylor y Poston 2007). Se han propuesto procesos epigenéticos para explicar los largos períodos de tiempo entre la exposición y el inicio de la enfermedad: si las exposiciones durante los primeros períodos de vulnerabilidad epigenética influyen en el estado epigenético, las marcas epigenéticas resultantes pueden mantenerse establemente en los linajes celulares para influir en la susceptibilidad de la enfermedad años más tarde. Waterland y Jirtle (2004) y Lillycrop (2011) discutieron recientemente datos experimentales que abordan la plausibilidad de tales mecanismos. La investigación humana descrita aquí proporciona datos correlativos. Las asociaciones entre el historial de exposición y el estado epigenético se describen en la sección anterior, mientras que las asociaciones entre el estado epigenético y el riesgo de enfermedad se describen a continuación, con algunos estudios que informan asociaciones sobre la exposición: estado epigenético y continuo de la enfermedad.
Condiciones reproductivas
La posibilidad de que el estado epigenético pueda influir en el éxito reproductivo se reconoció una vez que la investigación en organismos modelo reveló que la reprogramación epigenética dramática ocurre durante la gametogénesis, la fertilización y el desarrollo del cigoto, el embrión y la placenta (Feng et al. 2010). Las consideraciones éticas tienen estudios limitados que miden directamente el estado epigenético a un pequeño subconjunto de tipos celulares relevantes y etapas de desarrollo. Aquí revisamos los datos seleccionados que abordan la hipótesis de que los fenómenos epigenéticos pueden influir en el riesgo de infertilidad, trastornos del desarrollo y función de la placenta y peso al nacer.
La supervivencia fetal, el desarrollo y el crecimiento dependen de la placenta. A partir de la TE relativamente hipometilada, las células de la placenta en desarrollo se someten a una extensa metilación del ADN de novo (Serman et al. 2007). La regulación epigenética de los cambios en la función placentaria durante la gestación (revisado en Nelissen et al. 2011), acompañada por un proceso dinámico de pérdida de impronta postulado, tiene un papel importante en la maduración y función de la placenta (Pozharny et al. 2010). Se postula que las funciones placentarias no identificadas dependen de la impronta, porque los genes impresos se expresan abundantemente en la placenta, en comparación con otros órganos, y la impronta surgió durante la evolución de los mamíferos (Nelissen et al. 2011). La función placentaria perturbada puede causar restricción del crecimiento intrauterino (RCIU), un predictor de mala salud en el período neonatal y en la infancia, que también puede predisponer a enfermedades de la edad adulta.
Asma
La evidencia emergente sugiere que el estado epigenético puede contribuir a la patogénesis del asma. El asma es una reacción de hipersensibilidad de tipo I mediada por IgE que involucra una programación sesgada de linfocitos T CD4 + sin tratamiento previo hacia un linaje Th2 (Durham et al. 2011).
Enfermedades metabólicas
Se han observado cambios epigenéticos funcionales en la obesidad (Campion et al. 2009), diabetes (Reddy y Natarajan 2011), enfermedad cardiovascular (Wierda et al. 2010) y la constelación de anomalías conocidas como síndrome metabólico (Bruce and Hanson 2010). Por ejemplo, los efectos vasculares adversos de la hiperglucemia pueden continuar durante varios años después de un control glucémico suficiente, un fenómeno llamado memoria metabólica (Siebel et al. 2010), y hay evidencia de estudios en animales de que este efecto está asociado con cambios epigenéticos en el promotor de la subunidad NFκβ del gen p65 en las células endoteliales aórticas (El-Osta et al. 2008) y el aumento de la acetilación en H3K9 / K14 en varios genes implicados en la disfunción endotelial y la inflamación crónica (Pirola et al. 2011).
Desórdenes neurológicos
Históricamente, el campo de la epigenética se ha centrado en los mecanismos de dilucidación para mantener la metilación del ADN en células en división. Sin embargo, un trabajo reciente ha descubierto cambios dinámicos en la metilación del ADN en células que no se dividen, incluidas las neuronas (revisado en Mill et al. 2008), que motivan los estudios de los efectos de las exposiciones ambientales en las marcas epigenéticas en relación con los trastornos neurológicos.
La enfermedad de Alzheimer, la esquizofrenia y los trastornos del espectro autista muestran diversas anomalías epigenéticas (Akbarian 2010; Mill et al. 2008; Nguyen et al. 2010b; Schroeder et al. 2011). Se ha propuesto un mecanismo epigenético para explicar la asociación entre la hambruna durante el período prenatal y el riesgo de esquizofrenia (Lumey et al. 2011), así como las asociaciones entre la expresión de genes impresos y el autismo y la esquizofrenia (Badcock y Crespi 2008).
Cáncer
La metilación anormal del ADN, las modificaciones del código de histonas y los cambios de miARN se han demostrado en células cancerosas humanas según se revisó en otra parte (Kanwal y Gupta 2011; Lovat et al. 2011; Sharma et al. 2010). En los tumores malignos, se observa una hipometilación gradual del ADN en todo el genoma, concurrente con la hipermetilación en islas CpG normalmente no metiladas (Baylin y Jones 2011; Feinberg 2007). Aunque inicialmente no se reconoció una asociación directa entre la hiper y la hipo-metilación (Bariol et al. 2003; Iacopetta et al. 2007), un trabajo reciente sugiere que los dos fenómenos pueden estar bien relacionados y se limitan a compartimentos similares del genoma (Berman et al. 2012).
Aunque no se ha demostrado una correlación directa entre los niveles de nutrientes maternos de un solo carbono y la metilación aberrante del ADN en tumores infantiles o adultos, estos estudios proporcionan una base para futuras investigaciones sobre la relación entre la exposición prenatal a nutrientes asociados a la metilación y los eventos anormales de metilación. tan común en la carcinogénesis.
Fenómenos transgeneracionales.
En teoría, las marcas epigenéticas en los linajes de células somáticas podrían transmitirse a las células hijas durante la vida útil de un individuo expuesto, mientras que las marcas establecidas en los miembros del linaje de células germinales podrían transmitirse a las generaciones posteriores. A continuación se describen varios ejemplos de transmisión aparente de un insulto ambiental a través de generaciones. Sin embargo, si los mecanismos epigenéticos median estos fenómenos sigue siendo muy controvertido (Bollati y Baccarelli 2010). La evidencia convincente de que un mecanismo epigenético es responsable de los efectos transgeneracionales requiere la determinación del fenotipo en al menos tres generaciones después de la exposición. Tomando como F0 a la madre embarazada expuesta, se requieren observaciones de las generaciones F1 a F3 para excluir la posibilidad de efectos directos de la exposición tanto en células somáticas de la generación F1 como en progenitores de células germinales de los cuales surgirá la generación F2, ya que ambos son Presente durante el embarazo expuesto (Perera y Herbstman 2011). También es posible que la selección de embarazos para la viabilidad pueda influir en la distribución de genes que influyen en las marcas epigenéticas.
Animales experimentales
El ejemplo mejor documentado de la especificación transgeneracional de un fenotipo a través de la metilación del ADN es la determinación del color del pelaje y otros rasgos (obesidad, diabetes y tumores) en ratones agutí. Las respuestas que llevan el Avial epiallele metaestable (que a su vez que el patrón de pelaje agutí) tienen más probabilidades de ser descendientes, mientras que las represas de la misma cepa sin la Epiallele Avy (que tienen capas amarillas) tienen más de producir descendencia amarilla. Un gradiente continuo en el color del pelaje está relacionado con la penetrancia del epialele Avy (Morgan et al. 1999; Waterland y Jirtle 2003). La genisteína del fitoestrógeno también puede cambiar el estado epigenético de este alelo durante varias generaciones posteriores (Cropley et al. 2006; Dolinoy et al. 2007a; Lillycrop et al. 2005). Si bien estas observaciones argumentan de manera convincente la determinación epigenética del fenotipo agutí, el epialele Avy metaestable surgió de la inserción de un retrotransposón en el lugar de la exposición ambiental convencional.
En un modelo separado, la exposición experimental de ratas preñadas a agentes disruptores endocrinos (vinclozolina, bisfenol A), los cambios en la infertilidad masculina, el peso corporal y el riesgo de cáncer en las cuatro partes posteriores (Anway et al. 2005; Skinner 2008). Sin embargo, no se ha establecido si las marcas epigenéticas determinan este fenotipo a través de estas generaciones.
Estudios humanos
Hambruna
Pembrey et al. (2006) describieron una asociación entre la exposición del abuelo paterno a la hambruna en el norte de Suecia y la mortalidad en sus nietos, mientras que el suministro de alimentos de la abuela paterna se asoció en lugar de la mortalidad en sus nietas. Lumey (1992) informó efectos sobre el peso al nacer hasta dos generaciones después del hambre holandés en la Segunda Guerra Mundial.
Humo de tabaco
El Estudio de Salud Infantil del Sur de California ha demostrado un efecto del hábito de fumar en las abuelas durante el embarazo en el riesgo de asma de sus nietos, luego de controlar el hábito de fumar materno y la exposición ambiental al humo de tabaco (Li et al. 2005). Pembrey et al. (2006) también describieron los efectos del tabaquismo paterno preadolescente en el IMC en hijos pero no en hijas. Aunque cualquiera de estos fenómenos podría deberse a mecanismos epigenéticos, la mutación en el ADN en sí sería una alternativa plausible, como se ha demostrado para el humo de tabaco convencional (Yauk et al. 2007).
Dietilestilbestrol (DES)
Décadas atrás, se descubrió que los machos humanos expuestos en el útero al DES presentaban malformaciones urogenitales en exceso, incluidas las hipospadias (Henderson et al. 1976; Vessey et al. 1983; Whitehead y Leiter 1981), y posteriormente se informó una prevalencia elevada de hipospadias niños no expuestos cuyas madres habían estado expuestas en el útero al DES (Brouwers et al. 2006; Klip et al. 2002; Palmer et al. 2005; Pons et al. 2005). Más recientemente, en un estudio que abordó los efectos competitivos potenciales de factores ambientales y genotípicos medidos, se informó un exceso notable de hipospadias entre los nietos no expuestos de mujeres que habían estado expuestas en el útero al DES (Kalfa et al. 2011). Un mecanismo postulado para estas observaciones es que los cambios epigenéticos en el gen del receptor de andrógenos se inducen en células germinales primordiales de fetos femeninos expuestos al DES en el momento en que se forma el sistema reproductivo, y posteriormente se transmiten de generación en generación a hijos y nietos afectados (Kalfa et al. al. 2011). A nuestro entender, este mecanismo no ha sido examinado a nivel molecular.
Retos metodológicos
Asesoramiento de exposición
Los largos periodos de inducción entre la exposición y la aparición de muchas enfermedades que los mecanismos epigenéticos se proponen para mediar presentan desafíos notables para una evaluación precisa de las exposiciones ambientales. La mayoría de las exposiciones pueden cambiar con el tiempo, lo que complica la recuperación y la evaluación precisas de los biomarcadores de vida corta. Distinguir las exposiciones de duración limitada o los períodos de relevancia específica (por ejemplo, en el útero) de las exposiciones crónicas puede proporcionar una especificidad útil para abordar algunas preguntas de investigación. Los biomarcadores persistentes (por ejemplo, los niveles de plomo en los huesos), cuando están disponibles, son prometedores si el período específico de exposición no es crucial. La exposición evaluada prospectivamente y estrechamente vinculada a los períodos propuestos de vulnerabilidad del epigenoma (por ejemplo, períodos de invasión placentaria o especificación del sexo en el útero) sería ideal. Sin embargo, esto rara vez ocurre en entornos epidemiológicos con suficiente poder para detectar la mayoría de las asociaciones de enfermedades. Sin embargo, la estimación de las asociaciones exposición-estado epigenético puede ser más factible.
Tecnologias de laboratorio
Muestras biológicas
Métodos estadísticos
Varios autores (Furrow et al. 2011; Slatkin 2009; Tal et al. 2010) han desarrollado modelos de herencia epigenética que permiten restablecer el estado epigenético entre generaciones, así como inducción ambiental y modificaciones sensibles al ambiente. Han demostrado que la variación en el estado ambiental o epigenético podría producir una alta heredabilidad, comparable a la heredabilidad esperada de los efectos puramente genéticos. Sin embargo, estos documentos se centran más en la evaluación teórica de cuánto de la “heredabilidad perdida” podría deberse a la epigenética en lugar de proporcionar métodos para el análisis de datos epidemiológicos. Por lo tanto, resumimos brevemente un marco general que podría utilizarse para este último propósito. Los detalles y los estudios de simulación de apoyo se describirán completamente en otra parte.
Para abordar los fenómenos transgeneracionales, proponemos una extensión de este enfoque ilustrado en la Fig. 2. En este modelo, los efectos genéticos y ambientales de los abuelos (Gmm, Emm, etc.) se transmiten a los padres a través de epigenotipos transmitidos (Gmm *, etc.), que son modificados por el entorno de los padres y, a su vez, se transmiten a la generación de descendientes para determinar sus fenotipos, en combinación con sus propias exposiciones en la etapa de desarrollo relevante.
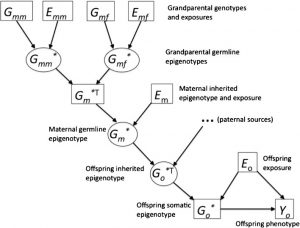
Figura 2
Representación esquemática del modelo de efectos transgeneracionales.
Extendiéndose a toda la escala del genoma
Gran parte del trabajo inicial sobre el papel de la epigenética en la enfermedad se ha centrado en la metilación global, las regiones metiladas diferencialmente asociadas con varios loci impresos o las regiones promotoras de los genes candidatos seleccionados.
En primer lugar, el uso de diseños retrospectivos de casos y controles introduce la posibilidad de una “causa inversa”, en la que la enfermedad o su tratamiento causa cambios epigenéticos en lugar de lo contrario. En segundo lugar, la especificidad tisular y celular de las marcas epigenéticas medidas en EWAS plantean los problemas de recolección e interpretación de muestras descritos en la sección anterior.
Oportunidades epidemiológicas
A pesar de la riqueza de la investigación sobre el papel de la epigenética en la enfermedad, ha habido mucha menos actividad sobre los determinantes ambientales de los cambios epigenéticos y su papel del estado epigenético en la mediación de las relaciones de exposición-respuesta, ya sea dentro de los individuos o entre generaciones. Rakyan et al. (2011) proporcionan una excelente revisión de algunos de los problemas de diseño en epidemiología epigenética. Aquí nos centramos en algunas oportunidades para un estudio epidemiológico adicional en esta área.
Estudios gemelos
En contraste con los estudios observacionales de singletons, los estudios de gemelos pueden proporcionar varias ventajas para los estudios de epigenética (Bell y Saffery 2012). Los gemelos monocigóticos se combinan con la edad, el genoma completo, el entorno infantil y el entorno cultural. Por el contrario, incluso los gemelos monocigóticos pueden considerarse solo parcialmente pareados en el entorno intrauterino. Debido a que los eventos epigenéticos ocurren en varios puntos a lo largo de la gestación, el estado epigenético al nacer probablemente esté influenciado por la corionicidad y posiblemente también por las características del amnio y la anatomía de la implantación.
Las diferencias entre los estados epigenéticos globales y específicos de genes de gemelos adultos idénticos se han descrito en numerosos estudios (Bell et al. 2012; Bocklandt et al. 2011; Boks et al. 2009; Fraga et al. 2005; Heijmans et al. 2007 ), sugiriendo que el estado epigenético cambia con la edad, o más exactamente, con la cohorte, ya que estas eran personas diferentes. El estado de metilación en algunos sitios CpG es altamente predictivo, como se muestra en un estudio reciente que identificó numerosas marcas de metilo en el ADN aislado de la saliva como altamente asociadas con la edad. En un conjunto de validación de participantes del estudio, el estado de metilación en solo dos de los sitios CpG identificados explicó el 73% de la varianza en la edad en un rango de 5 décadas (Bocklandt et al. 2011). Dichas marcas epigenéticas pueden resultar útiles no solo para comprender el proceso biológico asociado con el envejecimiento, sino también como herramientas para clasificar a los participantes en la investigación en grupos de edad con base biológica. Por ejemplo, se puede considerar que los individuos con grandes diferencias entre la edad predicha epigenéticamente y la edad cronológica tienen un estado fisiológico inusual o una bio-edad.
Estudios multigeneracionales
En el resto de esta sección, analizamos algunos de los ajustes de exposición únicos que podrían ser útiles para explorar el papel de la epigenética en los fenómenos de exposición transgeneracional aparentes.
Cohortes de hambre
La incidencia del cáncer de testículo ha aumentado durante décadas, y los análisis de cohortes de edad-período- demuestran sistemáticamente que el año de nacimiento es un determinante importante del riesgo de cáncer testicular. Según estos hallazgos, se postula que la exposición a causas ambientales no identificadas aumenta, y los efectos observados de la cohorte de nacimientos se atribuyen a la acción temprana de tales exposiciones. La excepción singular a este patrón es una caída en la incidencia entre los hombres nacidos en Europa durante la Segunda Guerra Mundial (Moller et al. 1995). Los mecanismos epigenéticos postulados relacionados con la ingesta de energía en los períodos in utero y perinatal justifican la investigación entre individuos gestados durante la hambruna y sus descendientes.
Estudios de salud y desarrollo infantil.
Los Estudios de Salud y Desarrollo Infantil de California (Cohn 2011; van den Berg et al. 1988) se iniciaron entre 1959 y 1967 con la inscripción de una cohorte de aproximadamente 20,000 embarazos, con seguimiento de los padres y los hijos hasta el día de hoy. Los padres y el niño proporcionaron muestras biológicas en el momento de la inscripción, junto con información limitada sobre el cuestionario sobre la exposición de los abuelos, y también se obtuvieron muestras longitudinales. Como estos niños ahora tienen más de 50 años, muchos han tenido hijos, también se han inscrito en el estudio, y los nietos ya están empezando a nacer. Esta cohorte representa, por lo tanto, una oportunidad única para estudiar fenómenos epigenéticos transgeneracionales, como sus estudios de exposición materna al DDT.
Descendientes de dietilestilbestrol
El DES es considerado como un potencial disruptor endocrino ambiental por muchos investigadores debido a que este compuesto se une a los receptores de hormonas esteroides y tiene solo fuentes exógenas. Debido a que la exposición ocurrió solo en entornos clínicos relativamente controlados, las cohortes de individuos expuestos en teoría podrían brindar una oportunidad para rastrear cualquier efecto epigenético de la exposición entre ellos y sus descendientes a los períodos de tiempo restringidos de sus embarazos o gestaciones antes de que la administración a mujeres embarazadas terminara en 1970s. Los datos de los grupos de exposición y comparación de calidad variable son o podrían estar disponibles a partir de varias fuentes, la más alta calidad en teoría son los participantes en los ensayos de eficacia de DES realizados en la década de 1950 (Dieckmann et al. 1953; Ferguson 1953), aunque los tamaños de muestra fueron limitados . No obstante, los numerosos conjuntos de casos y controles, cohortes expuestas al DES y grupos de interés que posteriormente reclutaron a un gran número de hombres y mujeres expuestos para monitorear e investigar los efectos en la salud de los individuos expuestos (Swan 2000) podrían resultar ser recursos valiosos para la investigación de posibles Efectos epigenéticos y transgeneracionales del DES entre individuos expuestos y sus descendientes. Los estudios iniciales de prueba de concepto podrían incluir la investigación de marcas epigenéticas postuladas que se hayan interrumpido por las exposiciones al DES.
Tecnologías de reproducción asistida.
En los países industrializados, 1 a 4% de los neonatos ahora son concebidos por ART. La vigilancia intensiva de la salud a largo plazo de estos niños ha revelado un aumento en la aparición de numerosos trastornos (Savage et al. 2011). Sin embargo, un próximo paso deseable en esta investigación —determinar si los procedimientos de tratamiento antirretroviral o las indicaciones para estos procedimientos (infertilidad o subfertilidad de los padres) tienen en cuenta el exceso de riesgo— está muy limitado por la escasez de datos sobre niños con antecedentes de solo uno de estos factores. Los mecanismos epigenéticos suelen postularse tanto para el tratamiento antirretroviral como para los orígenes paternos de varias afecciones asociadas con el tratamiento antirretroviral, incluidos los trastornos de la impronta del modelo y el IUGR. Por lo tanto, los nuevos estudios que apuntan a rastrear las marcas epigenéticas candidatas de las células relevantes del padre (por ejemplo, el esperma del padre) hasta los de los niños afectados por el TAR (por ejemplo, la placenta de los bebés con RCIU o las células somáticas de los niños con síndrome de Prader-Willi) parecen una Primer paso lógico para separar los efectos del tratamiento de la indicación. De manera más general, los estudios que comparan el estado epigenético de células relevantes de niños concebidos por ART con el de tipos de células similares de niños concebidos naturalmente pueden proporcionar información adicional con respecto a las condiciones en el desarrollo temprano, particularmente condiciones sobre representadas entre niños concebidos por ART. La vigilancia continua sin duda revelará si las condiciones de inicio tardío se agregan a esta lista a medida que las cohortes de niños concebidos por ART alcanzan edades en riesgo de enfermedades de la edad adulta. Una extensión lógica de esta vigilancia sería determinar entre los descendientes la presencia de fenotipos relevantes y marcas epigenéticas.
Conclusiones
Los resultados experimentales notables, tomados en conjunto, indican que los procesos epigenéticos podrían mediar plausiblemente los efectos de las exposiciones ambientales para influir en la susceptibilidad de la enfermedad en los mamíferos, ya que (1) las exposiciones específicas indujeron cambios medibles en el estado epigenético, (2) se demostró que el nuevo estado epigenético persiste después de la cesación de exposición, y (3) el fenotipo medible se asoció con cambios relacionados con la exposición en el estado epigenético. Un cuarto elemento, la alteración inducida por la exposición de marcas epigenéticas del ADN del linaje de células germinales, parece necesario para la transmisión transgeneracional de cambios epigenéticos inducidos por el medio ambiente. En este contexto, interpretamos datos observacionales humanos que ilustran asociaciones de exposiciones al estado epigenético y estado epigenético a la enfermedad para indicar que los mecanismos epigenéticos pueden mediar plausiblemente los efectos de la exposición en una amplia gama de enfermedades humanas.
Quizás el mayor significado de esta línea de investigación es el potencial para diseñar intervenciones novedosas articuladas por Dolinoy y Jirtle (2008):
a diferencia de las mutaciones genéticas, los perfiles epigenéticos son potencialmente reversibles. Por lo tanto, se pueden desarrollar enfoques epigenéticos para la prevención y el tratamiento, como suplementos nutricionales y / o terapias farmacéuticas para contrarrestar los perfiles epigenómicos negativos.
Como ejemplo, Huang et al. (2012) han desarrollado una terapia para reactivar el alelo Ube3a que se silencia epigenéticamente en el síndrome de Angelman. Sin embargo, antes de comenzar a materializar este potencial de traducción, es necesario realizar mucha investigación a lo largo de vías paralelas.
Necesitamos entender mejor los mecanismos epigenéticos básicos que operan durante períodos seleccionados cuando el epigenoma puede ser particularmente vulnerable a exposiciones ambientales (por ejemplo, períodos prenatales y postnatales tempranos, niñez, pubertad), así como mecanismos que habitualmente mantienen los estados epigenéticos apropiados. También debemos comprender los mecanismos relevantes para los efectos acumulativos de la exposición y las asociaciones con el envejecimiento, ya que la duración de la exposición y el envejecimiento son colineales. Una mejor comprensión de los mecanismos básicos en diferentes momentos de la vida guiaría los estudios de epidemiología genética para seleccionar las exposiciones ambientales que tienen mayor probabilidad de afectar los procesos epigenéticos, identificar los periodos de exposición más relevantes, identificar biomarcadores de la exposición y sugerir intermedios biológicos para estudiar.
Puede ser útil deconstruir más deliberadamente los pasos por los cuales una exposición ambiental puede afectar el riesgo de enfermedad a través de mecanismos epigenéticos. Por ejemplo, los estudios de asociación de exposiciones ambientales con eventos epigenéticos seleccionados como puntos finales (en lugar de intermedios en una vía compleja) pueden ser fructíferos y probablemente nos ayuden a concebir estudios para dilucidar una vía completa, desde una exposición que actúe al menos en Parte a través de mecanismos epigenéticos para el riesgo de enfermedad.
A medida que avancemos, será importante considerar seriamente las exposiciones ambientales a estudiar, ya que desearemos seleccionar las exposiciones candidatas más prometedoras (aquellas con mayor probabilidad de afectar los procesos epigenéticos), midiendo estas exposiciones en períodos de tiempo relevantes y con una precisión razonable. Además, no podemos ignorar las influencias genéticas en los procesos epigenéticos. Vemos más arriba que los estudios del estado epigenético de genes candidatos específicos están dando resultados interesantes y más estudios de este tipo están justificados. Dado el conocimiento limitado de esta interfaz genético-epigenética, para complementar el enfoque del gen candidato, se deben contemplar enfoques genómicos integradores para combinar los datos GWAS con datos epigenómicos. Claramente, se requerirán enfoques estadísticos y bioinformáticos para permitir la realización eficiente de estos análisis, especialmente a medida que nos expandimos a escala del genoma. De manera similar, se necesitará investigación sobre diseños de estudios factibles y eficientes, similares a la investigación actual sobre diseños óptimos para estudios basados en secuenciación. Finalmente, al igual que con otros campos emergentes (por ejemplo, la estandarización de los criterios de prueba para la inestabilidad de microsatélites o MSI), la estandarización de la terminología y los protocolos de prueba facilitarán la comunicación futura de hipótesis, enfoques científicos y resultados.
Artículo en PDF
Environmental epigenetics prospects for studying epigenetic mediation of exposure–response relationshipsReferencias
- Adli M, Bernstein BE. Whole-genome chromatin profiling from limited numbers of cells using nano-ChIP-seq. Nat Protoc. 2011;6:1656–1668. doi: 10.1038/nprot.2011.402. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Ainsworth HF, Unwin J, Jamison DL, Cordell HJ. Investigation of maternal effects, maternal-fetal interactions and parent-of-origin effects (imprinting), using mothers and their offspring. Genet Epidemiol. 2011;35:19–45. doi: 10.1002/gepi.20547. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Akbarian S. Epigenetics of schizophrenia. Curr Top Behav Neurosci. 2010;4:611–628. doi: 10.1007/7854_2010_38. [PubMed] [CrossRef] [Google Scholar]
- Andersen AN, Pinborg A, Loft A. Neonatal outcome in singletons conceived after ART. Lancet. 2008;372:694–695. doi: 10.1016/S0140-6736(08)61042-9. [PubMed] [CrossRef] [Google Scholar]
- Anway MD, Skinner MK. Transgenerational effects of the endocrine disruptor vinclozolin on the prostate transcriptome and adult onset disease. Prostate. 2008;68:517–529. doi: 10.1002/pros.20724. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Anway MD, Cupp AS, Uzumcu M, Skinner MK. Epigenetic transgenerational actions of endocrine disruptors and male fertility. Science. 2005;308:1466–1469. doi: 10.1126/science.1108190. [PubMed] [CrossRef] [Google Scholar]
- Apostolidou S, Abu-Amero S, O’Donoghue K, Frost J, Olafsdottir O, Chavele KM, Whittaker JC, Loughna P, Stanier P, Moore GE. Elevated placental expression of the imprinted PHLDA2 gene is associated with low birth weight. J Mol Med (Berlin) 2007;85:379–387. doi: 10.1007/s00109-006-0131-8. [PubMed] [CrossRef] [Google Scholar]
- Arita A, Niu J, Qu Q, Zhao N, Ruan Y, Nadas A, Chervona Y, Wu F, Sun H, Hayes RB, Costa M. Global levels of histone modifications in peripheral blood mononuclear cells of subjects with exposure to nickel. Environ Health Perspect. 2011;120:198–203. doi: 10.1289/ehp.1104140. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Aryee MJ, Wu Z, Ladd-Acosta C, Herb B, Feinberg AP, Yegnasubramanian S, Irizarry RA. Accurate genome-scale percentage DNA methylation estimates from microarray data. Biostatistics. 2011;12:197–210. doi: 10.1093/biostatistics/kxq055. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Baccarelli A, Bollati V. Epigenetics and environmental chemicals. Curr Opin Pediatr. 2009;21:243–251. doi: 10.1097/MOP.0b013e32832925cc. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Baccarelli A, Wright RO, Bollati V, Tarantini L, Litonjua AA, Suh HH, Zanobetti A, Sparrow D, Vokonas PS, Schwartz J. Rapid DNA methylation changes after exposure to traffic particles. Am J Respir Crit Care Med. 2009;179:572–578. doi: 10.1164/rccm.200807-1097OC. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Badcock C, Crespi B. Battle of the sexes may set the brain. Nature. 2008;454:1054–1055. doi: 10.1038/4541054a. [PubMed] [CrossRef] [Google Scholar]
- Baranzini SE, Mudge J, Velkinburgh JC, Khankhanian P, Khrebtukova I, Miller NA, Zhang L, Farmer AD, Bell CJ, Kim RW, May GD, Woodward JE, Caillier SJ, McElroy JP, Gomez R, Pando MJ, Clendenen LE, Ganusova EE, Schilkey FD, Ramaraj T, Khan OA, Huntley JJ, Luo S, Kwok PY, Wu TD, Schroth GP, Oksenberg JR, Hauser SL, Kingsmore SF. Genome, epigenome and RNA sequences of monozygotic twins discordant for multiple sclerosis. Nature. 2010;464:1351–1356. doi: 10.1038/nature08990. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bariol C, Suter C, Cheong K, Ku SL, Meagher A, Hawkins N, Ward R. The relationship between hypomethylation and CpG island methylation in colorectal neoplasia. Am J Pathol. 2003;162:1361–1371. doi: 10.1016/S0002-9440(10)63932-6. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Barker DJ, Gluckman PD, Godfrey KM, Harding JE, Owens JA, Robinson JS. Fetal nutrition and cardiovascular disease in adult life. Lancet. 1993;341:938–941. doi: 10.1016/0140-6736(93)91224-A. [PubMed] [CrossRef] [Google Scholar]
- Bayarsaihan D. Epigenetic mechanisms in inflammation. J Dent Res. 2011;90:9–17. doi: 10.1177/0022034510378683. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Baylin SB, Jones PA. A decade of exploring the cancer epigenome—biological and translational implications. Nat Rev Cancer. 2011;11:726–734. doi: 10.1038/nrc3130. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Begemann M, Spengler S, Kanber D, Haake A, Baudis M, Leisten I, Binder G, Markus S, Rupprecht T, Segerer H, Fricke-Otto S, Muhlenberg R, Siebert R, Buiting K, Eggermann T. Silver-Russell patients showing a broad range of ICR1 and ICR2 hypomethylation in different tissues. Clin Genet. 2011;80:83–88. doi: 10.1111/j.1399-0004.2010.01514.x. [PubMed] [CrossRef] [Google Scholar]
- Bell JT, Saffery R. The value of twins in epigenetic epidemiology. Int J Epidemiol. 2012;41:140–150. doi: 10.1093/ije/dyr179. [PubMed] [CrossRef] [Google Scholar]
- Bell JT, Pai AA, Pickrell JK, Gaffney DJ, Pique-Regi R, Degner JF, Gilad Y, Pritchard JK. DNA methylation patterns associate with genetic and gene expression variation in HapMap cell lines. Genome Biol. 2011;12:R10. doi: 10.1186/gb-2011-12-1-r10. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bell O, Tiwari VK, Thoma NH, Schubeler D. Determinants and dynamics of genome accessibility. Nat Rev Genet. 2011;12:554–564. doi: 10.1038/nrg3017. [PubMed] [CrossRef] [Google Scholar]
- Bell JT, Tsai PC, Yang TP, Pidsley R, Nisbet J, Glass D, Mangino M, Zhai G, Zhang F, Valdes A, Shin SY, Dempster EL, Murray RM, Grundberg E, Hedman AK, Nica A, Small KS, Dermitzakis ET, McCarthy MI, Mill J, Spector TD, Deloukas P. Epigenome-wide scans identify differentially methylated regions for age and age-related phenotypes in a healthy ageing population. PLoS Genet. 2012;8:e1002629. doi: 10.1371/journal.pgen.1002629. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Benchaib M, Ajina M, Lornage J, Niveleau A, Durand P, Guerin JF. Quantitation by image analysis of global DNA methylation in human spermatozoa and its prognostic value in in vitro fertilization: a preliminary study. Fertil Steril. 2003;80:947–953. doi: 10.1016/S0015-0282(03)01151-8. [PubMed] [CrossRef] [Google Scholar]
- Benchaib M, Braun V, Ressnikof D, Lornage J, Durand P, Niveleau A, Guerin JF. Influence of global sperm DNA methylation on IVF results. Hum Reprod. 2005;20:768–773. doi: 10.1093/humrep/deh684. [PubMed] [CrossRef] [Google Scholar]
- Berman BP, Weisenberger DJ, Aman JF, Hinoue T, Ramjan Z, Liu Y, Noushmehr H, Lange CPE, van Dijk CM, Tollenaar RAEM, Van Den Berg D, Laird PW (2011) Regions of focal DNA hypermethylation and long-range hypomethylation in colorectal cancer coincide with nuclear lamina–associated domains. Nat Genet 43 (in press) [PMC free article] [PubMed]
- Berman BP, Weisenberger DJ, Aman JF, Hinoue T, Ramjan Z, Liu Y, Noushmehr H, Lange CP, Dijk CM, Tollenaar RA, Berg D, Laird PW. Regions of focal DNA hypermethylation and long-range hypomethylation in colorectal cancer coincide with nuclear lamina-associated domains. Nat Genet. 2012;44:40–46. doi: 10.1038/ng.969. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Beyan H, Drexhage RC, Heul Nieuwenhuijsen L, Wit H, Padmos RC, Schloot NC, Drexhage HA, Leslie RD. Monocyte gene-expression profiles associated with childhood-onset type 1 diabetes and disease risk: a study of identical twins. Diabetes. 2010;59:1751–1755. doi: 10.2337/db09-1433. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Birney E, Lieb JD, Furey TS, Crawford GE, Iyer VR. Allele-specific and heritable chromatin signatures in humans. Hum Mol Genet. 2010;19:R204–R209. doi: 10.1093/hmg/ddq404. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bjornsson HT, Sigurdsson MI, Fallin MD, Irizarry RA, Aspelund T, Cui H, Yu W, Rongione MA, Ekstrom TJ, Harris TB, Launer LJ, Eiriksdottir G, Leppert MF, Sapienza C, Gudnason V, Feinberg AP. Intra-individual change over time in DNA methylation with familial clustering. JAMA. 2008;299:2877–2883. doi: 10.1001/jama.299.24.2877. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bocklandt S, Lin W, Sehl ME, Sanchez FJ, Sinsheimer JS, Horvath S, Vilain E. Epigenetic predictor of age. PLoS One. 2011;6:e14821. doi: 10.1371/journal.pone.0014821. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Boggs BA, Cheung P, Heard E, Spector DL, Chinault AC, Allis CD. Differentially methylated forms of histone H3 show unique association patterns with inactive human X chromosomes. Nat Genet. 2002;30:73–76. doi: 10.1038/ng787. [PubMed] [CrossRef] [Google Scholar]
- Boks MP, Derks EM, Weisenberger DJ, Strengman E, Janson E, Sommer IE, Kahn RS, Ophoff RA. The relationship of DNA methylation with age, gender and genotype in twins and healthy controls. PLoS One. 2009;4:e6767. doi: 10.1371/journal.pone.0006767. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bollati V, Baccarelli A. Environmental epigenetics. Heredity. 2010;105:105–112. doi: 10.1038/hdy.2010.2. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Bollati V, Baccarelli A, Hou L, Bonzini M, Fustinoni S, Cavallo D, Byun HM, Jiang J, Marinelli B, Pesatori AC, Bertazzi PA, Yang AS. Changes in DNA methylation patterns in subjects exposed to low-dose benzene. Cancer Res. 2007;67:876–880. doi: 10.1158/0008-5472.CAN-06-2995. [PubMed] [CrossRef] [Google Scholar]
- Bollati V, Marinelli B, Apostoli P, Bonzini M, Nordio F, Hoxha M, Pegoraro V, Motta V, Tarantini L, Cantone L, Schwartz J, Bertazzi PA, Baccarelli A. Exposure to metal-rich particulate matter modifies the expression of candidate microRNAs in peripheral blood leukocytes. Environ Health Perspect. 2010;118:763–768. doi: 10.1289/ehp.0901300. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Breitling LP, Yang R, Korn B, Burwinkel B, Brenner H. Tobacco-smoking-related differential DNA methylation: 27K discovery and replication. Am J Hum Genet. 2011;88:450–457. doi: 10.1016/j.ajhg.2011.03.003. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Breitling LP, Salzmann K, Rothenbacher D, Burwinkel B, Brenner H (2012) Smoking, F2RL3 methylation, and prognosis in stable coronary heart disease. Eur Heart J [Epub ahead of print] [PubMed]
- Breton CV, Byun HM, Wenten M, Pan F, Yang A, Gilliland FD. Prenatal tobacco smoke exposure affects global and gene-specific DNA methylation. Am J Respir Crit Care Med. 2009;180:462–467. doi: 10.1164/rccm.200901-0135OC. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Breton CV, Byun HM, Wang X, Salam MT, Siegmund K, Gilliland FD. DNA methylation in the arginase-nitric oxide synthase pathway is associated with exhaled nitric oxide in children with asthma. Am J Respir Crit Care Med. 2011;184:191–197. doi: 10.1164/rccm.201012-2029OC. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Breton CV, Salam MT, Gilliland FD. Heritability and role for the environment in DNA methylation in AXL receptor tyrosine kinase. Epigenetics. 2011;6:895–898. doi: 10.4161/epi.6.7.15768. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Breton CV, Salam MT, Gilliland FD. Heritability and role for the environment in DNA methylation in AXL receptor tyrosine kinase. Epigenetics. 2011;6:895–898. doi: 10.4161/epi.6.7.15768. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Brouwers MM, Feitz WF, Roelofs LA, Kiemeney LA, Gier RP, Roeleveld N. Hypospadias: a transgenerational effect of diethylstilbestrol? Hum Reprod. 2006;21:666–669. doi: 10.1093/humrep/dei398. [PubMed] [CrossRef] [Google Scholar]
- Bruce KD, Hanson MA. The developmental origins, mechanisms, and implications of metabolic syndrome. J Nutr. 2010;140:648–652. doi: 10.3945/jn.109.111179. [PubMed] [CrossRef] [Google Scholar]
- Burdge GC, Slater-Jefferies J, Torrens C, Phillips ES, Hanson MA, Lillycrop KA. Dietary protein restriction of pregnant rats in the F0 generation induces altered methylation of hepatic gene promoters in the adult male offspring in the F1 and F2 generations. Br J Nutr. 2007;97:435–439. doi: 10.1017/S0007114507352392. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Byun HM, Siegmund KD, Pan F, Weisenberger DJ, Kanel G, Laird PW, Yang AS. Epigenetic profiling of somatic tissues from human autopsy specimens identifies tissue- and individual-specific DNA methylation patterns. Hum Mol Genet. 2009;18:4808–4817. doi: 10.1093/hmg/ddp445. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Campion J, Milagro FI, Martinez JA. Individuality and epigenetics in obesity. Obes Rev. 2009;10:383–392. doi: 10.1111/j.1467-789X.2009.00595.x. [PubMed] [CrossRef] [Google Scholar]
- Cantone L, Nordio F, Hou L, Apostoli P, Bonzini M, Tarantini L, Angelici L, Bollati V, Zanobetti A, Schwartz J, Bertazzi PA, Baccarelli A. Inhalable metal-rich air particles and histone H3K4 dimethylation and H3K9 acetylation in a cross-sectional study of steel workers. Environ Health Perspect. 2011;119:964–969. doi: 10.1289/ehp.1002955. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Carrell DT, Hammoud SS. The human sperm epigenome and its potential role in embryonic development. Mol Hum Reprod. 2010;16:37–47. doi: 10.1093/molehr/gap090. [PubMed] [CrossRef] [Google Scholar]
- Chan TL, Yuen ST, Kong CK, Chan YW, Chan AS, Ng WF, Tsui WY, Lo MW, Tam WY, Li VS, Leung SY. Heritable germline epimutation of MSH2 in a family with hereditary nonpolyposis colorectal cancer. Nat Genet. 2006;38:1178–1183. doi: 10.1038/ng1866. [PubMed] [CrossRef] [Google Scholar]
- Chanda S, Dasgupta UB, Guhamazumder D, Gupta M, Chaudhuri U, Lahiri S, Das S, Ghosh N, Chatterjee D. DNA hypermethylation of promoter of gene p53 and p16 in arsenic-exposed people with and without malignancy. Toxicol Sci. 2006;89:431–437. doi: 10.1093/toxsci/kfj030. [PubMed] [CrossRef] [Google Scholar]
- Christensen BC, Marsit CJ. Epigenomics in environmental health. Front Genet. 2011;2:84. [PMC free article] [PubMed] [Google Scholar]
- Ciappio ED, Mason JB, Crott JW. Maternal one-carbon nutrient intake and cancer risk in offspring. Nutr Rev. 2011;69:561–571. doi: 10.1111/j.1753-4887.2011.00424.x. [PubMed] [CrossRef] [Google Scholar]
- Clifford H, Wessely F, Pendurthi S, Emes RD. Comparison of clustering methods for investigation of genome-wide methylation array data. Front Genet. 2011;2:88. [PMC free article] [PubMed] [Google Scholar]
- Cohn BA. Developmental and environmental origins of breast cancer: DDT as a case study. Reprod Toxicol. 2011;31:302–311. doi: 10.1016/j.reprotox.2010.10.004. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Coolen MW, Statham AL, Qu W, Campbell MJ, Henders AK, Montgomery GW, Martin NG, Clark SJ. Impact of the genome on the epigenome is manifested in DNA methylation patterns of imprinted regions in monozygotic and dizygotic twins. PLoS One. 2011;6:e25590. doi: 10.1371/journal.pone.0025590. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Cortessis VC (2009) Imprinting errors and in vitro fertilization. In: Carrell DT, Racowski C, Van Voorhis B, Schlegel P (eds) Biennial review of infertility, vol 1. Springer/Humana, Europe, pp 239–246
- Cortessis VK, Siegmund K, Houshdaran S, Laird PW, Sokol RZ. Repeated assessment by high-throughput assay demonstrates that sperm DNA methylation levels are highly reproducible. Fertil Steril. 2011;96:1325–1330. doi: 10.1016/j.fertnstert.2011.09.036. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Cropley JE, Suter CM, Beckman KB, Martin DI. Germ-line epigenetic modification of the murine A vy allele by nutritional supplementation. Proc Nat Acad Sci. 2006;103:17308–17312. doi: 10.1073/pnas.0607090103. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Curtin K, Slattery ML, Samowitz WS. CpG island methylation in colorectal cancer: past, present and future. Pathol Res Int. 2011;2011:902674. [PMC free article] [PubMed] [Google Scholar]
- D’Angelo DV, Whitehead N, Helms K, Barfield W, Ahluwalia IB. Birth outcomes of intended pregnancies among women who used assisted reproductive technology, ovulation stimulation, or no treatment. Fertil Steril. 2011;96(314–320):e2. [PubMed] [Google Scholar]
- Davey Smith G, Ebrahim S. Mendelian randomization: prospects, potentials, and limitations. Int J Epidemiol. 2004;33:30–42. doi: 10.1093/ije/dyh132. [PubMed] [CrossRef] [Google Scholar]
- Dempster EL, Pidsley R, Schalkwyk LC, Owens S, Georgiades A, Kane F, Kalidindi S, Picchioni M, Kravariti E, Toulopoulou T, Murray RM, Mill J. Disease-associated epigenetic changes in monozygotic twins discordant for schizophrenia and bipolar disorder. Hum Mol Genet. 2011;20:4786–4796. doi: 10.1093/hmg/ddr416. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Dieckmann WJ, Davis ME, Rynkiewicz LM, Pottinger RE. Does the administration of diethylstilbestrol during pregnancy have therapeutic value? Am J Obstet Gynecol. 1953;66:1062–1081. [PubMed] [Google Scholar]
- Diergaarde B, Braam H, Muijen GN, Ligtenberg MJ, Kok FJ, Kampman E. Dietary factors and microsatellite instability in sporadic colon carcinomas. Cancer Epidemiol Biomarkers Prev. 2003;12:1130–1136. [PubMed] [Google Scholar]
- Diplas AI, Lambertini L, Lee MJ, Sperling R, Lee YL, Wetmur J, Chen J. Differential expression of imprinted genes in normal and IUGR human placentas. Epigenetics. 2009;4:235–240. [PubMed] [Google Scholar]
- Dolinoy DC, Jirtle RL. Environmental epigenomics in human health and disease. Environ Mol Mutagen. 2008;49:4–8. doi: 10.1002/em.20366. [PubMed] [CrossRef] [Google Scholar]
- Dolinoy DC, Huang D, Jirtle RL. Maternal nutrient supplementation counteracts bisphenol A-induced DNA hypomethylation in early development. Proc Nat Acad Sci. 2007;104:13056–13061. doi: 10.1073/pnas.0703739104. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Dolinoy DC, Weidman JR, Jirtle RL. Epigenetic gene regulation: linking early developmental environment to adult disease. Reprod Toxicol. 2007;23:297–307. doi: 10.1016/j.reprotox.2006.08.012. [PubMed] [CrossRef] [Google Scholar]
- Durham AL, Wiegman C, Adcock IM. Epigenetics of asthma. Biochim Biophys Acta. 2011;1810:1103–1109. doi: 10.1016/j.bbagen.2011.03.006. [PubMed] [CrossRef] [Google Scholar]
- Eaton AM, Sandler R, Carethers JM, Millikan RC, Galanko J, Keku TO. 5,10-methylenetetrahydrofolate reductase 677 and 1298 polymorphisms, folate intake, and microsatellite instability in colon cancer. Cancer Epidemiol Biomarkers Prev. 2005;14:2023–2029. doi: 10.1158/1055-9965.EPI-05-0131. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Hajj N, Zechner U, Schneider E, Tresch A, Gromoll J, Hahn T, Schorsch M, Haaf T. Methylation status of imprinted genes and repetitive elements in sperm DNA from infertile males. Sex Dev. 2011;5:60–69. doi: 10.1159/000323806. [PubMed] [CrossRef] [Google Scholar]
- Elashoff RM, Li G, Li N. An approach to joint analysis of longitudinal measurements and competing risks failure time data. Stat Med. 2007;26:2813–2835. doi: 10.1002/sim.2749. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- El-Osta A, Brasacchio D, Yao D, Pocai A, Jones PL, Roeder RG, Cooper ME, Brownlee M. Transient high glucose causes persistent epigenetic changes and altered gene expression during subsequent normoglycemia. J Exp Med. 2008;205:2409–2417. doi: 10.1084/jem.20081188. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Enokida H, Shiina H, Urakami S, Terashima M, Ogishima T, Li LC, Kawahara M, Nakagawa M, Kane CJ, Carroll PR, Igawa M, Dahiya R. Smoking influences aberrant CpG hypermethylation of multiple genes in human prostate carcinoma. Cancer. 2006;106:79–86. doi: 10.1002/cncr.21577. [PubMed] [CrossRef] [Google Scholar]
- Estecio MR, Gallegos J, Vallot C, Castoro RJ, Chung W, Maegawa S, Oki Y, Kondo Y, Jelinek J, Shen L, Hartung H, Aplan PD, Czerniak BA, Liang S, Issa JP. Genome architecture marked by retrotransposons modulates predisposition to DNA methylation in cancer. Genome Res. 2010;20:1369–1382. doi: 10.1101/gr.107318.110. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Faulk C, Dolinoy DC. Timing is everything: the when and how of environmentally induced changes in the epigenome of animals. Epigenetics. 2011;6:791–797. doi: 10.4161/epi.6.7.16209. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Feinberg AP. Phenotypic plasticity and the epigenetics of human disease. Nature. 2007;447:433–440. doi: 10.1038/nature05919. [PubMed] [CrossRef] [Google Scholar]
- Feltus FA, Lee EK, Costello JF, Plass C, Vertino PM. DNA motifs associated with aberrant CpG island methylation. Genomics. 2006;87:572–579. doi: 10.1016/j.ygeno.2005.12.016. [PubMed] [CrossRef] [Google Scholar]
- Feng S, Jacobsen SE, Reik W. Epigenetic reprogramming in plant and animal development. Science. 2010;330:622–627. doi: 10.1126/science.1190614. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Ferguson JH. Effect of stilbestrol on pregnancy compared to the effect of a placebo. Am J Obstet Gynecol. 1953;65:592–601. [PubMed] [Google Scholar]
- Ferguson-Smith AC. Genomic imprinting: the emergence of an epigenetic paradigm. Nat Rev Genet. 2011;12:565–575. doi: 10.1038/nrg3032. [PubMed] [CrossRef] [Google Scholar]
- Fields PE, Kim ST, Flavell RA. Cutting edge: changes in histone acetylation at the IL-4 and IFN-gamma loci accompany Th1/Th2 differentiation. J Immunol. 2002;169:647–650. [PubMed] [Google Scholar]
- Filipponi D, Feil R. Perturbation of genomic imprinting in oligozoospermia. Epigenetics. 2009;4:27–30. doi: 10.4161/epi.4.1.7311. [PubMed] [CrossRef] [Google Scholar]
- Flom JD, Ferris JS, Liao Y, Tehranifar P, Richards CB, Cho YH, Gonzalez K, Santella RM, Terry MB. Prenatal smoke exposure and genomic DNA methylation in a multiethnic birth cohort. Cancer Epidemiol Biomarkers Prev. 2011;20:2518–2523. doi: 10.1158/1055-9965.EPI-11-0553. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Fortier AL, Lopes FL, Darricarrere N, Martel J, Trasler JM. Superovulation alters the expression of imprinted genes in the midgestation mouse placenta. Hum Mol Genet. 2008;17:1653–1665. doi: 10.1093/hmg/ddn055. [PubMed] [CrossRef] [Google Scholar]
- Fraga MF, Ballestar E, Paz MF, Ropero S, Setien F, Ballestar ML, Heine-Suner D, Cigudosa JC, Urioste M, Benitez J, Boix-Chornet M, Sanchez-Aguilera A, Ling C, Carlsson E, Poulsen P, Vaag A, Stephan Z, Spector TD, Wu YZ, Plass C, Esteller M. Epigenetic differences arise during the lifetime of monozygotic twins. Proc Nat Acad Sci. 2005;102:10604–10609. doi: 10.1073/pnas.0500398102. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Furrow RE, Christiansen FB, Feldman MW. Environment-sensitive epigenetics and the heritability of complex diseases. Genetics. 2011;189:1377–1387. doi: 10.1534/genetics.111.131912. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Galetzka D, Hansmann T, El Hajj N, Weis E, Irmscher B, Ludwig M, Schneider-Raetzke B, Kohlschmidt N, Beyer V, Bartsch O, Zechner U, Spix C, Haaf T (2012) Monozygotic twins discordant for constitutive BRCA1 promoter methylation, childhood cancer and secondary cancer. Epigenetics 7:47–54 [PMC free article] [PubMed]
- Gao Y, He Z, Wang Z, Luo Y, Sun H, Zhou Y, Huang L, Li M, Fang Q, Jiang S. Increased expression and altered methylation of HERVWE1 in the human placentas of smaller fetuses from monozygotic, dichorionic, discordant twins. PLoS One. 2012;7:e33503. doi: 10.1371/journal.pone.0033503. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Gertz J, Varley KE, Reddy TE, Bowling KM, Pauli F, Parker SL, Kucera KS, Willard HF, Myers RM. Analysis of DNA methylation in a three-generation family reveals widespread genetic influence on epigenetic regulation. PLoS Genet. 2011;7:e1002228. doi: 10.1371/journal.pgen.1002228. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Gervin K, Hammero M, Akselsen HE, Moe R, Nygard H, Brandt I, Gjessing HK, Harris JR, Undlien DE, Lyle R. Extensive variation and low heritability of DNA methylation identified in a twin study. Genome Res. 2011;21:1813–1821. doi: 10.1101/gr.119685.110. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Gervin K, Vigeland MD, Mattingsdal M, Hammero M, Nygard H, Olsen AO, Brandt I, Harris JR, Undlien DE, Lyle R. DNA methylation and gene expression changes in monozygotic twins discordant for psoriasis: identification of epigenetically dysregulated genes. PLoS Genet. 2012;8:e1002454. doi: 10.1371/journal.pgen.1002454. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Gordon L, Joo JH, Andronikos R, Ollikainen M, Wallace EM, Umstad MP, Permezel M, Oshlack A, Morley R, Carlin JB, Saffery R, Smyth GK, Craig JM. Expression discordance of monozygotic twins at birth: effect of intrauterine environment and a possible mechanism for fetal programming. Epigenetics. 2011;6:579–592. doi: 10.4161/epi.6.5.15072. [PubMed] [CrossRef] [Google Scholar]
- Greenland S. An introduction to instrumental variables for epidemiologists. Int J Epidemiol. 2000;29:722–729. doi: 10.1093/ije/29.4.722. [PubMed] [CrossRef] [Google Scholar]
- Guo L, Choufani S, Ferreira J, Smith A, Chitayat D, Shuman C, Uxa R, Keating S, Kingdom J, Weksberg R. Altered gene expression and methylation of the human chromosome 11 imprinted region in small for gestational age (SGA) placentae. Dev Biol. 2008;320:79–91. doi: 10.1016/j.ydbio.2008.04.025. [PubMed] [CrossRef] [Google Scholar]
- Haas CS, Creighton CJ, Pi X, Maine I, Koch AE, Haines GK, Ling S, Chinnaiyan AM, Holoshitz J. Identification of genes modulated in rheumatoid arthritis using complementary DNA microarray analysis of lymphoblastoid B cell lines from disease-discordant monozygotic twins. Arthr Rheum. 2006;54:2047–2060. doi: 10.1002/art.21953. [PubMed] [CrossRef] [Google Scholar]
- Harris RA, Wang T, Coarfa C, Nagarajan RP, Hong C, Downey SL, Johnson BE, Fouse SD, Delaney A, Zhao Y, Olshen A, Ballinger T, Zhou X, Forsberg KJ, Gu J, Echipare L, O’Geen H, Lister R, Pelizzola M, Xi Y, Epstein CB, Bernstein BE, Hawkins RD, Ren B, Chung WY, Gu H, Bock C, Gnirke A, Zhang MQ, Haussler D, Ecker JR, Li W, Farnham PJ, Waterland RA, Meissner A, Marra MA, Hirst M, Milosavljevic A, Costello JF. Comparison of sequencing-based methods to profile DNA methylation and identification of monoallelic epigenetic modifications. Nat Biotechnol. 2010;28:1097–1105. doi: 10.1038/nbt.1682. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Harris RA, Nagy-Szakal D, Pedersen N, Opekun A, Bronsky J, Munkholm P, Jespersgaard C, Andersen P, Melegh B, Ferry G, Jess T, Kellermayer R (2012) Genome-wide peripheral blood leukocyte DNA methylation microarrays identified a single association with inflammatory bowel diseases. Inflamm Bowel Dis [Epub ahead of print] [PMC free article] [PubMed]
- Heijmans BT, Kremer D, Tobi EW, Boomsma DI, Slagboom PE. Heritable rather than age-related environmental and stochastic factors dominate variation in DNA methylation of the human IGF2/H19 locus. Hum Mol Genet. 2007;16:547–554. doi: 10.1093/hmg/ddm010. [PubMed] [CrossRef] [Google Scholar]
- Heijmans BT, Tobi EW, Stein AD, Putter H, Blauw GJ, Susser ES, Slagboom PE, Lumey LH. Persistent epigenetic differences associated with prenatal exposure to famine in humans. Proc Nat Acad Sci. 2008;105:17046–17049. doi: 10.1073/pnas.0806560105. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Henderson BE, Benton B, Cosgrove M, Baptista J, Aldrich J, Townsend D, Hart W, Mack TM. Urogenital tract abnormalities in sons of women treated with diethylstilbestrol. Pediatrics. 1976;58:505–507. [PubMed] [Google Scholar]
- Herceg Z, Paliwal A. Epigenetic mechanisms in hepatocellular carcinoma: how environmental factors influence the epigenome. Mutat Res. 2011;727:55–61. doi: 10.1016/j.mrrev.2011.04.001. [PubMed] [CrossRef] [Google Scholar]
- Hitchins MP, Rapkins RW, Kwok CT, Srivastava S, Wong JJ, Khachigian LM, Polly P, Goldblatt J, Ward RL. Dominantly inherited constitutional epigenetic silencing of MLH1 in a cancer-affected family is linked to a single nucleotide variant within the 5′UTR. Cancer Cell. 2011;20:200–213. doi: 10.1016/j.ccr.2011.07.003. [PubMed] [CrossRef] [Google Scholar]
- Ho SM. Environmental epigenetics of asthma: an update. J Allergy Clin Immunol. 2010;126:453–465. doi: 10.1016/j.jaci.2010.07.030. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Houshdaran S, Cortessis VK, Siegmund K, Yang A, Laird PW, Sokol RZ. Widespread epigenetic abnormalities suggest a broad DNA methylation erasure defect in abnormal human sperm. PLoS One. 2007;2:e1289. doi: 10.1371/journal.pone.0001289. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Huang Y, Chang X, Lee J, Cho YG, Zhong X, Park IS, Liu JW, Califano JA, Ratovitski EA, Sidransky D, Kim MS. Cigarette smoke induces promoter methylation of single-stranded DNA-binding protein 2 in human esophageal squamous cell carcinoma. Int J Cancer. 2011;128:2261–2273. doi: 10.1002/ijc.25569. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Huang HS, Allen JA, Mabb AM, King IF, Miriyala J, Taylor-Blake B, Sciaky N, Dutton JW, Jr, Lee HM, Chen X, Jin J, Bridges AS, Zylka MJ, Roth BL, Philpot BD. Topoisomerase inhibitors unsilence the dormant allele of Ube3a in neurons. Nature. 2012;481:185–189. doi: 10.1038/nature10726. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Hughes LA, Brandt PA, Bruine AP, Wouters KA, Hulsmans S, Spiertz A, Goldbohm RA, Goeij AF, Herman JG, Weijenberg MP, Engeland M. Early life exposure to famine and colorectal cancer risk: a role for epigenetic mechanisms. PLoS One. 2009;4:e7951. doi: 10.1371/journal.pone.0007951. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Iacopetta B, Grieu F, Phillips M, Ruszkiewicz A, Moore J, Minamoto T, Kawakami K. Methylation levels of LINE-1 repeats and CpG island loci are inversely related in normal colonic mucosa. Cancer Sci. 2007;98:1454–1460. doi: 10.1111/j.1349-7006.2007.00548.x. [PubMed] [CrossRef] [Google Scholar]
- Ideraabdullah FY, Abramowitz LK, Thorvaldsen JL, Krapp C, Wen SC, Engel N, Bartolomei MS. Novel cis-regulatory function in ICR-mediated imprinted repression of H19. Developmental biology. 2011;355:349–357. doi: 10.1016/j.ydbio.2011.04.036. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Jaffe AE, Feinberg AP, Irizarry RA, Leek JT. Significance analysis and statistical dissection of variably methylated regions. Biostatistics. 2012;13:166–178. doi: 10.1093/biostatistics/kxr013. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Jaffe AE, Murakami P, Lee H, Leek JT, Fallin MD, Feinberg AP, Irizarry RA. Bump hunting to identify differentially methylated regions in epigenetic epidemiology studies. Int J Epidemiol. 2012;41:200–209. doi: 10.1093/ije/dyr238. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Jardim MJ. microRNAs: implications for air pollution research. Mutat Res. 2011;717:38–45. doi: 10.1016/j.mrfmmm.2011.03.014. [PubMed] [CrossRef] [Google Scholar]
- Javierre BM, Fernandez AF, Richter J, Al-Shahrour F, Martin-Subero JI, Rodriguez-Ubreva J, Berdasco M, Fraga MF, O’Hanlon TP, Rider LG, Jacinto FV, Lopez-Longo FJ, Dopazo J, Forn M, Peinado MA, Carreno L, Sawalha AH, Harley JB, Siebert R, Esteller M, Miller FW, Ballestar E. Changes in the pattern of DNA methylation associate with twin discordance in systemic lupus erythematosus. Genome Res. 2010;20:170–179. doi: 10.1101/gr.100289.109. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Jiang G, Xu L, Song S, Zhu C, Wu Q, Zhang L, Wu L. Effects of long-term low-dose cadmium exposure on genomic DNA methylation in human embryo lung fibroblast cells. Toxicology. 2008;244:49–55. doi: 10.1016/j.tox.2007.10.028. [PubMed] [CrossRef] [Google Scholar]
- Jones B, Chen J. Inhibition of IFN-gamma transcription by site-specific methylation during T helper cell development. EMBO J. 2006;25:2443–2452. doi: 10.1038/sj.emboj.7601148. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kakiuchi C, Ishiwata M, Nanko S, Ozaki N, Iwata N, Umekage T, Tochigi M, Kohda K, Sasaki T, Imamura A, Okazaki Y, Kato T. Up-regulation of ADM and SEPX1 in the lymphoblastoid cells of patients in monozygotic twins discordant for schizophrenia. Am J Med Genet B Neuropsychiatr Genet. 2008;147B:557–564. doi: 10.1002/ajmg.b.30643. [PubMed] [CrossRef] [Google Scholar]
- Kalfa N, Paris F, Soyer-Gobillard MO, Daures JP, Sultan C. Prevalence of hypospadias in grandsons of women exposed to diethylstilbestrol during pregnancy: a multigenerational national cohort study. Fertil Steril. 2011;95:2574–2577. doi: 10.1016/j.fertnstert.2011.02.047. [PubMed] [CrossRef] [Google Scholar]
- Kaminsky Z, Petronis A, Wang SC, Levine B, Ghaffar O, Floden D, Feinstein A. Epigenetics of personality traits: an illustrative study of identical twins discordant for risk-taking behavior. Twin Res Hum Genet. 2008;11:1–11. doi: 10.1375/twin.11.1.1. [PubMed] [CrossRef] [Google Scholar]
- Kanwal R, Gupta S. Epigenetic modifications in cancer. Clin Genet. 2011;81:303–311. doi: 10.1111/j.1399-0004.2011.01809.x. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kerkel K, Spadola A, Yuan E, Kosek J, Jiang L, Hod E, Li K, Murty VV, Schupf N, Vilain E, Morris M, Haghighi F, Tycko B. Genomic surveys by methylation-sensitive SNP analysis identify sequence- dependent allele-specific DNA methylation. Nat Genet. 2008;40:904–908. doi: 10.1038/ng.174. [PubMed] [CrossRef] [Google Scholar]
- Keshet I, Schlesinger Y, Farkash S, Rand E, Hecht M, Segal E, Pikarski E, Young RA, Niveleau A, Cedar H, Simon I. Evidence for an instructive mechanism of de novo methylation in cancer cells. Nat Genet. 2006;38:149–153. doi: 10.1038/ng1719. [PubMed] [CrossRef] [Google Scholar]
- Kim DH, Nelson HH, Wiencke JK, Zheng S, Christiani DC, Wain JC, Mark EJ, Kelsey KT. p16(INK4a) and histology-specific methylation of CpG islands by exposure to tobacco smoke in non-small cell lung cancer. Cancer Res. 2001;61:3419–3424. [PubMed] [Google Scholar]
- Klip H, Verloop J, Gool JD, Koster ME, Burger CW, Leeuwen FE. Hypospadias in sons of women exposed to diethylstilbestrol in utero: a cohort study. Lancet. 2002;359:1102–1107. doi: 10.1016/S0140-6736(02)08152-7. [PubMed] [CrossRef] [Google Scholar]
- Kobayashi H, Sato A, Otsu E, Hiura H, Tomatsu C, Utsunomiya T, Sasaki H, Yaegashi N, Arima T. Aberrant DNA methylation of imprinted loci in sperm from oligospermic patients. Hum Mol Genet. 2007;16:2542–2551. doi: 10.1093/hmg/ddm187. [PubMed] [CrossRef] [Google Scholar]
- Koukoura O, Sifakis S, Soufla G, Zaravinos A, Apostolidou S, Jones A, Widschwendter M, Spandidos DA. Loss of imprinting and aberrant methylation of IGF2 in placentas from pregnancies complicated with fetal growth restriction. Int J Mol Med. 2011;28:481–487. [PubMed] [Google Scholar]
- Koukoura O, Sifakis S, Zaravinos A, Apostolidou S, Jones A, Hajiioannou J, Widschwendter M, Spandidos DA. Hypomethylation along with increased H19 expression in placentas from pregnancies complicated with fetal growth restriction. Placenta. 2011;32:51–57. doi: 10.1016/j.placenta.2010.10.017. [PubMed] [CrossRef] [Google Scholar]
- Kristensen LS, Wojdacz TK, Thestrup BB, Wiuf C, Hager H, Hansen LL. Quality assessment of DNA derived from up to 30 years old formalin fixed paraffin embedded (FFPE) tissue for PCR-based methylation analysis using SMART-MSP and MS-HRM. BMC Cancer. 2009;9:453. doi: 10.1186/1471-2407-9-453. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Kuratomi G, Iwamoto K, Bundo M, Kusumi I, Kato N, Iwata N, Ozaki N, Kato T. Aberrant DNA methylation associated with bipolar disorder identified from discordant monozygotic twins. Mol Psychiatry. 2008;13:429–441. doi: 10.1038/sj.mp.4002001. [PubMed] [CrossRef] [Google Scholar]
- Kwon NH, Kim JS, Lee JY, Oh MJ, Choi DC. DNA methylation and the expression of IL-4 and IFN-gamma promoter genes in patients with bronchial asthma. J Clin Immunol. 2008;28:139–146. doi: 10.1007/s10875-007-9148-1. [PubMed] [CrossRef] [Google Scholar]
- Laird PW. Principles and challenges of genome-wide DNA methylation analysis. Nat Rev Genet. 2010;11:191–203. doi: 10.1038/nrg2732. [PubMed] [CrossRef] [Google Scholar]
- Langevin SM, Houseman EA, Christensen BC, Wiencke JK, Nelson HH, Karagas MR, Marsit CJ, Kelsey KT. The influence of aging, environmental exposures and local sequence features on the variation of DNA methylation in blood. Epigenetics. 2011;6:908–919. doi: 10.4161/epi.6.7.16431. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Langevin SM, Koestler DC, Christensen BC, Butler RA, Wiencke JK, Nelson HH, Houseman EA, Marsit CJ, Kelsey KT. Peripheral blood DNA methylation profiles are indicative of head and neck squamous cell carcinoma: an epigenome-wide association study. Epigenetics. 2012;7:291–299. doi: 10.4161/epi.7.3.19134. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Lee H, Jaffe AE, Feinberg JI, Tryggvadottir R, Brown S, Montano C, Aryee MJ, Irizarry RA, Herbstman J, Witter FR, Goldman LR, Feinberg AP, Fallin MD. DNA methylation shows genome-wide association of NFIX, RAPGEF2 and MSRB3 with gestational age at birth. Int J Epidemiol. 2012;41:188–199. doi: 10.1093/ije/dyr237. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Li YF, Langholz B, Salam MT, Gilliland FD. Maternal and grandmaternal smoking patterns are associated with early childhood asthma. Chest. 2005;127:1232–1241. doi: 10.1378/chest.127.4.1232. [PubMed] [CrossRef] [Google Scholar]
- Li L, Wang L, Xu X, Lou H, Le F, Sheng J, Huang H, Jin F. Genome-wide DNA methylation patterns in IVF-conceived mice and their progeny: a putative model for ART-conceived humans. Reprod Toxicol. 2011;32:98–105. doi: 10.1016/j.reprotox.2011.05.016. [PubMed] [CrossRef] [Google Scholar]
- Lienert F, Wirbelauer C, Som I, Dean A, Mohn F, Schubeler D. Identification of genetic elements that autonomously determine DNA methylation states. Nat Genet. 2011;43:1091–1097. doi: 10.1038/ng.946. [PubMed] [CrossRef] [Google Scholar]
- Ligtenberg MJ, Kuiper RP, Chan TL, Goossens M, Hebeda KM, Voorendt M, Lee TY, Bodmer D, Hoenselaar E, Hendriks-Cornelissen SJ, Tsui WY, Kong CK, Brunner HG, Kessel AG, Yuen ST, Krieken JH, Leung SY, Hoogerbrugge N. Heritable somatic methylation and inactivation of MSH2 in families with Lynch syndrome due to deletion of the 3′ exons of TACSTD1. Nat Genet. 2009;41:112–117. doi: 10.1038/ng.283. [PubMed] [CrossRef] [Google Scholar]
- Lillycrop KA. Effect of maternal diet on the epigenome: implications for human metabolic disease. Proc Nutr Soc. 2011;70:64–72. doi: 10.1017/S0029665110004027. [PubMed] [CrossRef] [Google Scholar]
- Lillycrop KA, Phillips ES, Jackson AA, Hanson MA, Burdge GC. Dietary protein restriction of pregnant rats induces and folic acid supplementation prevents epigenetic modification of hepatic gene expression in the offspring. J Nutr. 2005;135:1382–1386. [PubMed] [Google Scholar]
- Lim U, Song M-A. Dietary and lifestyle factors of DNA methylation. In: Dumitrescu RG, Verma M, editors. Cancer epigenetics: methods and protocols, vol 863. Berlin: Springer Science & Bysubess Neduam LLC; 2012. [Google Scholar]
- Limsui D, Vierkant RA, Tillmans LS, Wang AH, Weisenberger DJ, Laird PW, Lynch CF, Anderson KE, French AJ, Haile RW, Harnack LJ, Potter JD, Slager SL, Smyrk TC, Thibodeau SN, Cerhan JR, Limburg PJ. Cigarette smoking and colorectal cancer risk by molecularly defined subtypes. J Natl Cancer Inst. 2010;102:1012–1022. doi: 10.1093/jnci/djq201. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Liu X, Nelson A, Wang X, Kanaji N, Kim M, Sato T, Nakanishi M, Li Y, Sun J, Michalski J, Patil A, Basma H, Rennard SI. MicroRNA-146a modulates human bronchial epithelial cell survival in response to the cytokine-induced apoptosis. Biochem Biophys Res Commun. 2009;380:177–182. doi: 10.1016/j.bbrc.2009.01.066. [PubMed] [CrossRef] [Google Scholar]
- Lovat F, Valeri N, Croce CM. MicroRNAs in the pathogenesis of cancer. Semin Oncol. 2011;38:724–733. doi: 10.1053/j.seminoncol.2011.08.006. [PubMed] [CrossRef] [Google Scholar]
- Lumey LH. Decreased birthweights in infants after maternal in utero exposure to the Dutch famine of 1944–1945. Paediatr Perinat Epidemiol. 1992;6:240–253. doi: 10.1111/j.1365-3016.1992.tb00764.x. [PubMed] [CrossRef] [Google Scholar]
- Lumey LH, Stein AD, Susser E. Prenatal famine and adult health. Annu Rev Public Health. 2011;32:237–262. doi: 10.1146/annurev-publhealth-031210-101230. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Madrigano J, Baccarelli A, Mittleman MA, Wright RO, Sparrow D, Vokonas PS, Tarantini L, Schwartz J. Prolonged exposure to particulate pollution, genes associated with glutathione pathways, and DNA methylation in a cohort of older men. Environ Health Perspect. 2011;119:977–982. doi: 10.1289/ehp.1002773. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Majumdar S, Chanda S, Ganguli B, Mazumder DN, Lahiri S, Dasgupta UB. Arsenic exposure induces genomic hypermethylation. Environ Toxicol. 2010;25:315–318. doi: 10.1002/tox.20497. [PubMed] [CrossRef] [Google Scholar]
- Marques CJ, Costa P, Vaz B, Carvalho F, Fernandes S, Barros A, Sousa M. Abnormal methylation of imprinted genes in human sperm is associated with oligozoospermia. Mol Hum Reprod. 2008;14:67–74. doi: 10.1093/molehr/gam093. [PubMed] [CrossRef] [Google Scholar]
- Marsit CJ, Karagas MR, Danaee H, Liu M, Andrew A, Schned A, Nelson HH, Kelsey KT. Carcinogen exposure and gene promoter hypermethylation in bladder cancer. Carcinogenesis. 2006;27:112–116. doi: 10.1093/carcin/bgi172. [PubMed] [CrossRef] [Google Scholar]
- Mastroeni D, McKee A, Grover A, Rogers J, Coleman PD. Epigenetic differences in cortical neurons from a pair of monozygotic twins discordant for Alzheimer’s disease. PLoS One. 2009;4:e6617. doi: 10.1371/journal.pone.0006617. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Matigian N, Windus L, Smith H, Filippich C, Pantelis C, McGrath J, Mowry B, Hayward N. Expression profiling in monozygotic twins discordant for bipolar disorder reveals dysregulation of the WNT signalling pathway. Mol Psychiatry. 2007;12:815–825. doi: 10.1038/sj.mp.4001998. [PubMed] [CrossRef] [Google Scholar]
- Mattes J, Collison A, Plank M, Phipps S, Foster PS. Antagonism of microRNA-126 suppresses the effector function of TH2 cells and the development of allergic airways disease. Proc Natl Acad Sci USA. 2009;106:18704–18709. doi: 10.1073/pnas.0905063106. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- McDaniell R, Lee BK, Song L, Liu Z, Boyle AP, Erdos MR, Scott LJ, Morken MA, Kucera KS, Battenhouse A, Keefe D, Collins FS, Willard HF, Lieb JD, Furey TS, Crawford GE, Iyer VR, Birney E. Heritable individual-specific and allele-specific chromatin signatures in humans. Science. 2010;328:235–239. doi: 10.1126/science.1184655. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- McDonald SD, Han Z, Mulla S, Murphy KE, Beyene J, Ohlsson A. Preterm birth and low birth weight among in vitro fertilization singletons: a systematic review and meta-analyses. Eur J Obstet Gynecol Reprod Biol. 2009;146:138–148. doi: 10.1016/j.ejogrb.2009.05.035. [PubMed] [CrossRef] [Google Scholar]
- McDonald SD, Han Z, Mulla S, Ohlsson A, Beyene J, Murphy KE. Preterm birth and low birth weight among in vitro fertilization twins: a systematic review and meta-analyses. Eur J Obstet Gynecol Reprod Biol. 2010;148:105–113. doi: 10.1016/j.ejogrb.2009.09.019. [PubMed] [CrossRef] [Google Scholar]
- McGrath J, Solter D. Completion of mouse embryogenesis requires both the maternal and paternal genomes. Cell. 1984;37:179–183. doi: 10.1016/0092-8674(84)90313-1. [PubMed] [CrossRef] [Google Scholar]
- McMinn J, Wei M, Schupf N, Cusmai J, Johnson EB, Smith AC, Weksberg R, Thaker HM, Tycko B. Unbalanced placental expression of imprinted genes in human intrauterine growth restriction. Placenta. 2006;27:540–549. doi: 10.1016/j.placenta.2005.07.004. [PubMed] [CrossRef] [Google Scholar]
- Mill J, Tang T, Kaminsky Z, Khare T, Yazdanpanah S, Bouchard L, Jia P, Assadzadeh A, Flanagan J, Schumacher A, Wang SC, Petronis A. Epigenomic profiling reveals DNA-methylation changes associated with major psychosis. Am J Hum Genet. 2008;82:696–711. doi: 10.1016/j.ajhg.2008.01.008. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Mitchell LE, Weinberg CR. Evaluation of offspring and maternal genetic effects on disease risk using a family-based approach: the “pent” design. Am J Epidemiol. 2005;162:676–685. doi: 10.1093/aje/kwi249. [PubMed] [CrossRef] [Google Scholar]
- Mitchell MM, Lleo A, Zammataro L, Mayo MJ, Invernizzi P, Bach N, Shimoda S, Gordon S, Podda M, Gershwin ME, Selmi C, LaSalle JM. Epigenetic investigation of variably X chromosome inactivated genes in monozygotic female twins discordant for primary biliary cirrhosis. Epigenetics. 2011;6:95–102. doi: 10.4161/epi.6.1.13405. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Molitor J, Marjoram P, Thomas DC. Fine-scale mapping of diseases with multiple mutations via spatial clustering techniques. Am J Hum Genet. 2003;73:1368–1384. doi: 10.1086/380415. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Moller H, Jorgensen N, Forman D. Trends in incidence of testicular cancer in boys and adolescent men. Int J Cancer. 1995;61:761–764. doi: 10.1002/ijc.2910610604. [PubMed] [CrossRef] [Google Scholar]
- Morgan HD, Sutherland HG, Martin DI, Whitelaw E. Epigenetic inheritance at the agouti locus in the mouse. Nat Genet. 1999;23:314–318. doi: 10.1038/15490. [PubMed] [CrossRef] [Google Scholar]
- Murphy SK, Adigun A, Huang Z, Overcash F, Wang F, Jirtle RL, Schildkraut JS, Murtha AP, Iversen ES, Hoyo C. Gender-specific methylation differences in relation to prenatal exposure to cigarette smoke. Gene. 2011;494:36–43. doi: 10.1016/j.gene.2011.11.062. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Nadeau K, McDonald-Hyman C, Noth EM, Pratt B, Hammond SK, Balmes J, Tager I. Ambient air pollution impairs regulatory T-cell function in asthma. J Allergy Clin Immunol. 2010;126:845–852. doi: 10.1016/j.jaci.2010.08.008. [PubMed] [CrossRef] [Google Scholar]
- Nagarajan RP, Hogart AR, Gwye Y, Martin MR, LaSalle JM. Reduced MeCP2 expression is frequent in autism frontal cortex and correlates with aberrant MECP2 promoter methylation. Epigenetics. 2006;1:e1–e11. doi: 10.4161/epi.1.4.3514. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Nan HM, Song YJ, Yun HY, Park JS, Kim H. Effects of dietary intake and genetic factors on hypermethylation of the hMLH1 gene promoter in gastric cancer. World J Gastroenterol. 2005;11:3834–3841. [PMC free article] [PubMed] [Google Scholar]
- Nana-Sinkam SP, Hunter MG, Nuovo GJ, Schmittgen TD, Gelinas R, Galas D, Marsh CB. Integrating the MicroRNome into the study of lung disease. Am J Respir Crit Care Med. 2009;179:4–10. doi: 10.1164/rccm.200807-1042PP. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Nelissen EC, Montfoort AP, Dumoulin JC, Evers JL. Epigenetics and the placenta. Hum Reprod Update. 2011;17:397–417. doi: 10.1093/humupd/dmq052. [PubMed] [CrossRef] [Google Scholar]
- Nguyen A, Rauch TA, Pfeifer GP, Hu VW. Global methylation profiling of lymphoblastoid cell lines reveals epigenetic contributions to autism spectrum disorders and a novel autism candidate gene, RORA, whose protein product is reduced in autistic brain. FASEB J. 2010;24:3036–3051. doi: 10.1096/fj.10-154484. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Oates NA, Vliet J, Duffy DL, Kroes HY, Martin NG, Boomsma DI, Campbell M, Coulthard MG, Whitelaw E, Chong S. Increased DNA methylation at the AXIN1 gene in a monozygotic twin from a pair discordant for a caudal duplication anomaly. Am J Hum Genet. 2006;79:155–162. doi: 10.1086/505031. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- O’Hanlon TP, Rider LG, Gan L, Fannin R, Paules RS, Umbach DM, Weinberg CR, Shah RR, Mav D, Gourley MF, Miller FW. Gene expression profiles from discordant monozygotic twins suggest that molecular pathways are shared among multiple systemic autoimmune diseases. Arthr Res Ther. 2011;13:R69. doi: 10.1186/ar3330. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Ohm JE, McGarvey KM, Yu X, Cheng L, Schuebel KE, Cope L, Mohammad HP, Chen W, Daniel VC, Yu W, Berman DM, Jenuwein T, Pruitt K, Sharkis SJ, Watkins DN, Herman JG, Baylin SB. A stem cell-like chromatin pattern may predispose tumor suppressor genes to DNA hypermethylation and heritable silencing. Nat Genet. 2007;39:237–242. doi: 10.1038/ng1972. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Ollikainen M, Smith KR, Joo EJ, Ng HK, Andronikos R, Novakovic B, Abdul Aziz NK, Carlin JB, Morley R, Saffery R, Craig JM. DNA methylation analysis of multiple tissues from newborn twins reveals both genetic and intrauterine components to variation in the human neonatal epigenome. Hum Mol Genet. 2010;19:4176–4188. doi: 10.1093/hmg/ddq336. [PubMed] [CrossRef] [Google Scholar]
- Pacheco SE, Houseman EA, Christensen BC, Marsit CJ, Kelsey KT, Sigman M, Boekelheide K. Integrative DNA methylation and gene expression analyses identify DNA packaging and epigenetic regulatory genes associated with low motility sperm. PLoS One. 2011;6:e20280. doi: 10.1371/journal.pone.0020280. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Palmer JR, Wise LA, Robboy SJ, Titus-Ernstoff L, Noller KL, Herbst AL, Troisi R, Hoover RN. Hypospadias in sons of women exposed to diethylstilbestrol in utero. Epidemiology. 2005;16:583–586. doi: 10.1097/01.ede.0000164789.59728.6d. [PubMed] [CrossRef] [Google Scholar]
- Patel CJ, Bhattacharya J, Butte AJ. An environment-wide association study (EWAS) on type 2 diabetes mellitus. PLoS One. 2010;5:e10746. doi: 10.1371/journal.pone.0010746. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Pauley KM, Chan EK. MicroRNAs and their emerging roles in immunology. Ann N Y Acad Sci. 2008;1143:226–239. doi: 10.1196/annals.1443.009. [PubMed] [CrossRef] [Google Scholar]
- Pavanello S, Bollati V, Pesatori AC, Kapka L, Bolognesi C, Bertazzi PA, Baccarelli A. Global and gene-specific promoter methylation changes are related to anti-B[a]PDE-DNA adduct levels and influence micronuclei levels in polycyclic aromatic hydrocarbon-exposed individuals. Int J Cancer. 2009;125:1692–1697. doi: 10.1002/ijc.24492. [PubMed] [CrossRef] [Google Scholar]
- Pembrey ME, Bygren LO, Kaati G, Edvinsson S, Northstone K, Sjostrom M, Golding J. Sex-specific, male-line transgenerational responses in humans. Eur J Hum Genet. 2006;14:159–166. doi: 10.1038/sj.ejhg.5201538. [PubMed] [CrossRef] [Google Scholar]
- Perera F, Herbstman J. Prenatal environmental exposures, epigenetics, and disease. Reprod Toxicol. 2011;31:363–373. doi: 10.1016/j.reprotox.2010.12.055. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Perera F, Tang WY, Herbstman J, Tang D, Levin L, Miller R, Ho SM. Relation of DNA methylation of 5′-CpG island of ACSL3 to transplacental exposure to airborne polycyclic aromatic hydrocarbons and childhood asthma. PLoS One. 2009;4:E4488. doi: 10.1371/journal.pone.0004488. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Pilsner JR, Hu H, Ettinger A, Sanchez BN, Wright RO, Cantonwine D, Lazarus A, Lamadrid-Figueroa H, Mercado-Garcia A, Tellez-Rojo MM, Hernandez-Avila M. Influence of prenatal lead exposure on genomic methylation of cord blood DNA. Environ Health Perspect. 2009;117:1466–1471. [PMC free article] [PubMed] [Google Scholar]
- Pirola L, Balcerczyk A, Tothill RW, Haviv I, Kaspi A, Lunke S, Ziemann M, Karagiannis T, Tonna S, Kowalczyk A, Beresford-Smith B, Macintyre G, Kelong M, Hongyu Z, Zhu J, El-Osta A. Genome-wide analysis distinguishes hyperglycemia regulated epigenetic signatures of primary vascular cells. Genome Res. 2011;21:1601–1615. doi: 10.1101/gr.116095.110. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Plagemann A, Harder T, Brunn M, Harder A, Roepke K, Wittrock-Staar M, Ziska T, Schellong K, Rodekamp E, Melchior K, Dudenhausen JW. Hypothalamic proopiomelanocortin promoter methylation becomes altered by early overfeeding: an epigenetic model of obesity and the metabolic syndrome. J Physiol. 2009;587:4963–4976. doi: 10.1113/jphysiol.2009.176156. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Pons JC, Papiernik E, Billon A, Hessabi M, Duyme M. Hypospadias in sons of women exposed to diethylstilbestrol in utero. Prenat Diagn. 2005;25:418–419. doi: 10.1002/pd.1136. [PubMed] [CrossRef] [Google Scholar]
- Pozharny Y, Lambertini L, Ma Y, Ferrara L, Litton CG, Diplas A, Jacobs AR, Chen J, Stone JL, Wetmur J, Lee MJ. Genomic loss of imprinting in first-trimester human placenta. Am J Obstet Gynecol. 2010;202(391):e1–e8. [PubMed] [Google Scholar]
- Ptashne M. On the use of the word ‘epigenetic’ Curr Biol. 2007;17:R233–R236. doi: 10.1016/j.cub.2007.02.030. [PubMed] [CrossRef] [Google Scholar]
- Rakyan VK, Down TA, Balding DJ, Beck S. Epigenome-wide association studies for common human diseases. Nat Rev Genet. 2011;12:529–541. doi: 10.1038/nrg3000. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Reddy MA, Natarajan R. Epigenetic mechanisms in diabetic vascular complications. Cardiovasc Res. 2011;90:421–429. doi: 10.1093/cvr/cvr024. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Relton CL, Davey Smith G. Two-step epigenetic Mendelian randomization: a strategy for establishing the causal role of epigenetic processes in pathways to disease. Int J Epidemiol. 2012;41:161–176. doi: 10.1093/ije/dyr233. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Rosa A, Picchioni MM, Kalidindi S, Loat CS, Knight J, Toulopoulou T, Vonk R, Schot AC, Nolen W, Kahn RS, McGuffin P, Murray RM, Craig IW. Differential methylation of the X-chromosome is a possible source of discordance for bipolar disorder female monozygotic twins. Am J Med Genet B Neuropsychiatr Genet. 2008;147B:459–462. doi: 10.1002/ajmg.b.30616. [PubMed] [CrossRef] [Google Scholar]
- Russo AL, Thiagalingam A, Pan H, Califano J, Cheng KH, Ponte JF, Chinnappan D, Nemani P, Sidransky D, Thiagalingam S. Differential DNA hypermethylation of critical genes mediates the stage-specific tobacco smoke-induced neoplastic progression of lung cancer. Clin Cancer Res. 2005;11:2466–2470. doi: 10.1158/1078-0432.CCR-04-1962. [PubMed] [CrossRef] [Google Scholar]
- Saffery R, Morley R, Carlin JB, Joo J-HE, Ollikainen M, Novakovic B, Andronikos R, Li X, Loke YJ, Carson N, Wallace EM, Umstad MP, Permezel M, Galati JC, Craig JM. Cohort profile: the peri/post-natal epigenetic twins study. Int J Epidemiol. 2011;41:55–61. doi: 10.1093/ije/dyr140. [PubMed] [CrossRef] [Google Scholar]
- Salam MT, Byun HM, Lurmann F, Breton CV, Wang X, Eckel SP, Gilliland FD. Genetic and epigenetic variations in inducible nitric oxide synthase promoter, particulate pollution, and exhaled nitric oxide levels in children. J Allergy Clin Immunol. 2012;129(232–239):e7. [PMC free article] [PubMed] [Google Scholar]
- Samowitz WS, Albertsen H, Sweeney C, Herrick J, Caan BJ, Anderson KE, Wolff RK, Slattery ML. Association of smoking, CpG island methylator phenotype, and V600E BRAF mutations in colon cancer. J Natl Cancer Inst. 2006;98:1731–1738. doi: 10.1093/jnci/djj468. [PubMed] [CrossRef] [Google Scholar]
- Sato A, Otsu E, Negishi H, Utsunomiya T, Arima T. Aberrant DNA methylation of imprinted loci in superovulated oocytes. Hum Reprod. 2007;22:26–35. doi: 10.1093/humrep/del316. [PubMed] [CrossRef] [Google Scholar]
- Savage T, Peek J, Hofman PL, Cutfield WS. Childhood outcomes of assisted reproductive technology. Hum Reprod. 2011;26:2392–2400. doi: 10.1093/humrep/der212. [PubMed] [CrossRef] [Google Scholar]
- Scesnaite A, Jarmalaite S, Mutanen P, Anttila S, Nyberg F, Benhamou S, Boffetta P, Husgafvel-Pursiainen K (2012) Similar DNA methylation pattern in lung tumours from smokers and never-smokers with second-hand tobacco smoke exposure. Mutagenesis [Epub ahead of print] [PubMed]
- Schalkwyk LC, Meaburn EL, Smith R, Dempster EL, Jeffries AR, Davies MN, Plomin R, Mill J. Allelic skewing of DNA methylation is widespread across the genome. Am J Hum Genet. 2010;86:196–212. doi: 10.1016/j.ajhg.2010.01.014. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Schernhammer ES, Giovannuccci E, Fuchs CS, Ogino S. A prospective study of dietary folate and vitamin B and colon cancer according to microsatellite instability and KRAS mutational status. Cancer Epidemiol Biomarkers Prev. 2008;17:2895–2898. doi: 10.1158/1055-9965.EPI-08-0638. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Schlesinger Y, Straussman R, Keshet I, Farkash S, Hecht M, Zimmerman J, Eden E, Yakhini Z, Ben-Shushan E, Reubinoff BE, Bergman Y, Simon I, Cedar H. Polycomb-mediated methylation on Lys27 of histone H3 pre-marks genes for de novo methylation in cancer. Nat Genet. 2007;39:232–236. doi: 10.1038/ng1950. [PubMed] [CrossRef] [Google Scholar]
- Schneider E, Pliushch G, Hajj N, Galetzka D, Puhl A, Schorsch M, Frauenknecht K, Riepert T, Tresch A, Muller AM, Coerdt W, Zechner U, Haaf T. Spatial, temporal and interindividual epigenetic variation of functionally important DNA methylation patterns. Nucleic Acids Res. 2010;38:3880–3890. doi: 10.1093/nar/gkq126. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Schroeder DI, Lott P, Korf I, LaSalle JM. Large-scale methylation domains mark a functional subset of neuronally expressed genes. Genome Res. 2011;21:1583–1591. doi: 10.1101/gr.119131.110. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Serman L, Vlahovic M, Sijan M, Bulic-Jakus F, Serman A, Sincic N, Matijevic R, Juric-Lekic G, Katusic A. The impact of 5-azacytidine on placental weight, glycoprotein pattern and proliferating cell nuclear antigen expression in rat placenta. Placenta. 2007;28:803–811. doi: 10.1016/j.placenta.2007.04.001. [PubMed] [CrossRef] [Google Scholar]
- Sharma S, Kelly TK, Jones PA. Epigenetics in cancer. Carcinogenesis. 2010;31:27–36. doi: 10.1093/carcin/bgp220. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Sharp AJ, Stathaki E, Migliavacca E, Brahmachary M, Montgomery SB, Dupre Y, Antonarakis SE. DNA methylation profiles of human active and inactive X chromosomes. Genome Res. 2011;21:1592–1600. doi: 10.1101/gr.112680.110. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Siebel AL, Fernandez AZ, El-Osta A. Glycemic memory associated epigenetic changes. Biochem Pharmacol. 2010;80:1853–1859. doi: 10.1016/j.bcp.2010.06.005. [PubMed] [CrossRef] [Google Scholar]
- Siegmund KD. Statistical approaches for the analysis of DNA methylation microarray data. Hum Genet. 2011;129:585–595. doi: 10.1007/s00439-011-0993-x. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Siegmund KD, Laird PW, Laird-Offringa IA. A comparison of cluster analysis methods using DNA methylation data. Bioinformatics. 2004;20:1896–1904. doi: 10.1093/bioinformatics/bth176. [PubMed] [CrossRef] [Google Scholar]
- Siegmund KD, Levine AJ, Chang J, Laird PW. Modeling exposures for DNA methylation profiles. Cancer Epidemiol Biomarkers Prev. 2006;15:567–572. doi: 10.1158/1055-9965.EPI-05-0717. [PubMed] [CrossRef] [Google Scholar]
- Sinclair KD, Young LE, Wilmut I, McEvoy TG. In utero overgrowth in ruminants following embryo culture: lessons from mice and a warning to men. Hum Reprod. 2000;15(Suppl 5):68–86. doi: 10.1093/humrep/15.suppl_5.68. [PubMed] [CrossRef] [Google Scholar]
- Slatkin M. Epigenetic inheritance and the missing heritability problem. Genetics. 2009;182:845–850. doi: 10.1534/genetics.109.102798. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Slattery ML, Anderson K, Curtin K, Ma KN, Schaffer D, Samowitz W. Dietary intake and microsatellite instability in colon tumors. Int J Cancer. 2001;93:601–607. doi: 10.1002/ijc.1370. [PubMed] [CrossRef] [Google Scholar]
- Slattery ML, Curtin K, Sweeney C, Levin TR, Potter JD, Wolff RK, Albertsen H, Samowitz W. Diet and lifestyle factor associations with CpG island methylator phenotype and BRAF mutations in colon cancer. Int J Cancer. 2006;120:656–663. doi: 10.1002/ijc.22342. [PubMed] [CrossRef] [Google Scholar]
- Su RC, Becker AB, Kozyrskyj AL, Hayglass KT. Epigenetic regulation of established human type 1 versus type 2 cytokine responses. J Allergy Clin Immunol. 2008;121(57–63):e3. [PubMed] [Google Scholar]
- Sundar IK, Caito S, Yao H, Rahman I. Oxidative stress, thiol redox signaling methods in epigenetics. Methods Enzymol. 2010;474:213–244. doi: 10.1016/S0076-6879(10)74013-1. [PubMed] [CrossRef] [Google Scholar]
- Suter CM, Martin DI, Ward RL. Germline epimutation of MLH1 in individuals with multiple cancers. Nat Genet. 2004;36:497–501. doi: 10.1038/ng1342. [PubMed] [CrossRef] [Google Scholar]
- Swan SH. Intrauterine exposure to diethylstilbestrol: long-term effects in humans. APMIS. 2000;108:793–804. doi: 10.1111/j.1600-0463.2000.tb00001.x. [PubMed] [CrossRef] [Google Scholar]
- Tal O, Kisdi E, Jablonka E. Epigenetic contribution to covariance between relatives. Genetics. 2010;184:1037–1050. doi: 10.1534/genetics.109.112466. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Talens RP, Boomsma DI, Tobi EW, Kremer D, Jukema JW, Willemsen G, Putter H, Slagboom PE, Heijmans BT. Variation, patterns, and temporal stability of DNA methylation: considerations for epigenetic epidemiology. FASEB J. 2010;24:3135–3144. doi: 10.1096/fj.09-150490. [PubMed] [CrossRef] [Google Scholar]
- Talens RP, Jukema JW, Trompet S, Kremer D, Westendorp RG, Lumey LH, Sattar N, Putter H, Slagboom PE, Heijmans BT. Hypermethylation at loci sensitive to the prenatal environment is associated with increased incidence of myocardial infarction. Int J Epidemiol. 2011;40:1–10. doi: 10.1093/ije/dyr032. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Tanay A, O’Donnell AH, Damelin M, Bestor TH. Hyperconserved CpG domains underlie Polycomb-binding sites. Proc Natl Acad Sci USA. 2007;104:5521–5526. doi: 10.1073/pnas.0609746104. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Tarantini L, Bonzini M, Apostoli P, Pegoraro V, Bollati V, Marinelli B, Cantone L, Rizzo G, Hou L, Schwartz J, Bertazzi PA, Baccarelli A. Effects of particulate matter on genomic DNA methylation content and iNOS promoter methylation. Environ Health Perspect. 2009;117:217–222. [PMC free article] [PubMed] [Google Scholar]
- Tarutani Y, Takayama S. Monoallelic gene expression and its mechanisms. Current opinion in plant biology. 2011;14:608–613. doi: 10.1016/j.pbi.2011.07.001. [PubMed] [CrossRef] [Google Scholar]
- Taylor PD, Poston L. Developmental programming of obesity in mammals. Exp Physiol. 2007;92:287–298. doi: 10.1113/expphysiol.2005.032854. [PubMed] [CrossRef] [Google Scholar]
- Terry MB, Delgado-Cruzata L, Vin-Raviv N, Wu HC, Santella RM. DNA methylation in white blood cells: association with risk factors in epidemiologic studies. Epigenetics. 2011;6:828–837. doi: 10.4161/epi.6.7.16500. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Teschendorff AE, Menon U, Gentry-Maharaj A, Ramus SJ, Weisenberger DJ, Shen H, Campan M, Noushmehr H, Bell CG, Maxwell AP, Savage DA, Mueller-Holzner E, Marth C, Kocjan G, Gayther SA, Jones A, Beck S, Wagner W, Laird PW, Jacobs IJ, Widschwendter M. Age-dependent DNA methylation of genes that are suppressed in stem cells is a hallmark of cancer. Genome Res. 2010;20:440–446. doi: 10.1101/gr.103606.109. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Thomson JP, Skene PJ, Selfridge J, Clouaire T, Guy J, Webb S, Kerr AR, Deaton A, Andrews R, James KD, Turner DJ, Illingworth R, Bird A. CpG islands influence chromatin structure via the CpG-binding protein Cfp1. Nature. 2010;464:1082–1086. doi: 10.1038/nature08924. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Tierling S, Souren NY, Reither S, Zang KD, Meng-Hentschel J, Leitner D, Oehl-Jaschkowitz B, Walter J. DNA methylation studies on imprinted loci in a male monozygotic twin pair discordant for Beckwith-Wiedemann syndrome. Clin Genet. 2011;79:546–553. doi: 10.1111/j.1399-0004.2010.01482.x. [PubMed] [CrossRef] [Google Scholar]
- Toyota M, Ahuja N, Ohe-Toyota M, Herman JG, Baylin SB, Issa JP. CpG island methylator phenotype in colorectal cancer. Proc Nat Acad Sci USA. 1999;96:8681–8686. doi: 10.1073/pnas.96.15.8681. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Trasler JM. Epigenetics in spermatogenesis. Mol Cell Endocrinol. 2009;306:33–36. doi: 10.1016/j.mce.2008.12.018. [PubMed] [CrossRef] [Google Scholar]
- Tycko B. Mapping allele-specific DNA methylation: a new tool for maximizing information from GWAS. Am J Hum Genet. 2010;86:109–112. doi: 10.1016/j.ajhg.2010.01.021. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Valinluck V, Tsai HH, Rogstad DK, Burdzy A, Bird A, Sowers LC. Oxidative damage to methyl-CpG sequences inhibits the binding of the methyl-CpG binding domain (MBD) of methyl-CpG binding protein 2 (MeCP2) Nucleic Acids Res. 2004;32:4100–4108. doi: 10.1093/nar/gkh739. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Berg BJ, Christianson RE, Oechsli FW. The California Child Health and Development Studies of the School of Public Health, University of California at Berkeley. Paediatr Perinat Epidemiol. 1988;2:265–282. doi: 10.1111/j.1365-3016.1988.tb00218.x. [PubMed] [CrossRef] [Google Scholar]
- Donk M, Engeland M, Pellis L, Witteman BJ, Kok FJ, Keijer J, Kampman E. Dietary folate intake in combination with MTHFR C677T genotype and promoter methylation of tumor suppressor and DNA repair genes in sporadic colorectal adenomas. Cancer Epidemiol Biomarkers Prev. 2007;16:327–333. doi: 10.1158/1055-9965.EPI-06-0810. [PubMed] [CrossRef] [Google Scholar]
- Guelpen B, Dahlin AM, Hultdin J, Eklof V, Johansson I, Henriksson ML, Cullman I, Hallmans G, Palmqvist R. One-carbon metabolism and CpG island methylator phenotype status in incident colorectal cancer: a nested case-referent study. Cancer Causes Control. 2010;21:557–566. doi: 10.1007/s10552-009-9484-y. [PubMed] [CrossRef] [Google Scholar]
- Montfoort AP, Hanssen LL, Sutter P, Viville S, Geraedts JP, Boer P. Assisted reproduction treatment and epigenetic inheritance. Hum Reprod Update. 2012;18:171–197. doi: 10.1093/humupd/dmr047. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Vermeulen SH, Shi M, Weinberg CR, Umbach DM. A hybrid design: case-parent triads supplemented by control-mother dyads. Genet Epidemiol. 2009;33:136–144. doi: 10.1002/gepi.20365. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Vessey MP, Fairweather DV, Norman-Smith B, Buckley J. A randomized double-blind controlled trial of the value of stilboestrol therapy in pregnancy: long-term follow-up of mothers and their offspring. Br J Obstet Gynaecol. 1983;90:1007–1017. doi: 10.1111/j.1471-0528.1983.tb06438.x. [PubMed] [CrossRef] [Google Scholar]
- Wark PA, Weijenberg MP, Veer P, Wijhe G, Luchtenborg M, Muijen GN, Goeij AF, Goldbohm RA, Brandt PA. Fruits, vegetables, and hMLH1 protein-deficient and -proficient colon cancer: the Netherlands cohort study. Cancer Epidemiol Biomarkers Prev. 2005;14:1619–1625. doi: 10.1158/1055-9965.EPI-05-0109. [PubMed] [CrossRef] [Google Scholar]
- Waterland RA, Jirtle RL. Transposable elements: targets for early nutritional effects on epigenetic gene regulation. Mol Cell Biol. 2003;23:5293–5300. doi: 10.1128/MCB.23.15.5293-5300.2003. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Waterland RA, Jirtle RL. Early nutrition, epigenetic changes at transposons and imprinted genes, and enhanced susceptibility to adult chronic diseases. Nutrition. 2004;20:63–68. doi: 10.1016/j.nut.2003.09.011. [PubMed] [CrossRef] [Google Scholar]
- Waterland RA, Kellermayer R, Laritsky E, Rayco-Solon P, Harris RA, Travisano M, Zhang W, Torskaya MS, Zhang J, Shen L, Manary MJ, Prentice AM. Season of conception in rural gambia affects DNA methylation at putative human metastable epialleles. PLoS Genet. 2010;6:e1001252. doi: 10.1371/journal.pgen.1001252. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Weaver IC, Cervoni N, Champagne FA, D’Alessio AC, Sharma S, Seckl JR, Dymov S, Szyf M, Meaney MJ. Epigenetic programming by maternal behavior. Nat Neurosci. 2004;7:847–854. doi: 10.1038/nn1276. [PubMed] [CrossRef] [Google Scholar]
- Weisenberger DJ, Siegmund KD, Campan M, Young J, Long TI, Faasse MA, Kang GH, Widschwendter M, Weener D, Buchanan D, Koh H, Simms L, Barker M, Leggett B, Levine J, Kim M, French AJ, Thibodeau SN, Jass J, Haile R, Laird PW. CpG island methylator phenotype underlies sporadic microsatellite instability and is tightly associated with BRAF mutation in colorectal cancer. Nat Genet. 2006;38:787–793. doi: 10.1038/ng1834. [PubMed] [CrossRef] [Google Scholar]
- Weth O, Renkawitz R. CTCF function is modulated by neighboring DNA binding factors. Biochem Cell Biol. 2011;89:459–468. doi: 10.1139/o11-033. [PubMed] [CrossRef] [Google Scholar]
- White GP, Watt PM, Holt BJ, Holt PG. Differential patterns of methylation of the IFN-gamma promoter at CpG and non-CpG sites underlie differences in IFN-gamma gene expression between human neonatal and adult CD45RO-T cells. J Immunol. 2002;168:2820–2827. [PubMed] [Google Scholar]
- Whitehead ED, Leiter E. Genital abnormalities and abnormal semen analyses in male patients exposed to diethylstilbestrol in utero. J Urol. 1981;125:47–50. [PubMed] [Google Scholar]
- Widschwendter M, Fiegl H, Egle D, Mueller-Holzner E, Spizzo G, Marth C, Weisenberger DJ, Campan M, Young J, Jacobs I, Laird PW. Epigenetic stem cell signature in cancer. Nat Genet. 2007;39(2):157–158. doi: 10.1038/ng1941. [PubMed] [CrossRef] [Google Scholar]
- Wierda RJ, Geutskens SB, Jukema JW, Quax PH, Elsen PJ. Epigenetics in atherosclerosis and inflammation. J Cell Mol Med. 2010;14:1225–1240. doi: 10.1111/j.1582-4934.2010.01022.x. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wilker EH, Baccarelli A, Suh H, Vokonas P, Wright RO, Schwartz J. Black carbon exposures, blood pressure, and interactions with single nucleotide polymorphisms in MicroRNA processing genes. Environ Health Perspect. 2010;118:943–948. doi: 10.1289/ehp.0901440. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wong CC, Caspi A, Williams B, Craig IW, Houts R, Ambler A, Moffitt TE, Mill J. A longitudinal study of epigenetic variation in twins. Epigenetics. 2010;5:516–526. doi: 10.4161/epi.5.6.12226. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wong CC, Caspi A, Williams B, Houts R, Craig IW, Mill J. A longitudinal twin study of skewed X chromosome-inactivation. PLoS One. 2011;6:e17873. doi: 10.1371/journal.pone.0017873. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wright RO, Baccarelli A. Metals and neurotoxicology. J Nutr. 2007;137:2809–2813. [PubMed] [Google Scholar]
- Wright RO, Schwartz J, Wright RJ, Bollati V, Tarantini L, Park SK, Hu H, Sparrow D, Vokonas P, Baccarelli A. Biomarkers of lead exposure and DNA methylation within retrotransposons. Environ Health Perspect. 2010;118:790–795. doi: 10.1289/ehp.0901429. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Wu HC, Delgado-Cruzata L, Flom JD, Kappil M, Ferris JS, Liao Y, Santella RM, Terry MB. Global methylation profiles in DNA from different blood cell types. Epigenetics. 2011;6:76–85. doi: 10.4161/epi.6.1.13391. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Yauk CL, Berndt ML, Williams A, Rowan-Carroll A, Douglas GR, Stampfli MR. Mainstream tobacco smoke causes paternal germ-line DNA mutation. Cancer Res. 2007;67:5103–5106. doi: 10.1158/0008-5472.CAN-07-0279. [PubMed] [CrossRef] [Google Scholar]
- Yauk C, Polyzos A, Rowan-Carroll A, Somers CM, Godschalk RW, Schooten FJ, Berndt ML, Pogribny IP, Koturbash I, Williams A, Douglas GR, Kovalchuk O. Germ-line mutations, DNA damage, and global hypermethylation in mice exposed to particulate air pollution in an urban/industrial location. Proc Nat Acad Sci. 2008;105:605–610. doi: 10.1073/pnas.0705896105. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Zhang L, Hou D, Chen X, Li D, Zhu L, Zhang Y, Li J, Bian Z, Liang X, Cai X, Yin Y, Wang C, Zhang T, Zhu D, Zhang D, Xu J, Chen Q, Ba Y, Liu J, Wang Q, Chen J, Wang J, Wang M, Zhang Q, Zhang J, Zen K, Zhang CY. Exogenous plant MIR168a specifically targets mammalian LDLRAP1: evidence of cross-kingdom regulation by microRNA. Cell Res. 2012;22:107–126. doi: 10.1038/cr.2011.158. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
- Zhou ZH, Lei YX, Wang CX. Analysis of aberrant methylation in DNA repair genes during malignant transformation of human bronchial epithelial cells induced by cadmium. Toxicol Sci. 2011;125:412–417. doi: 10.1093/toxsci/kfr320. [PubMed] [CrossRef] [Google Scholar]




